تحقیقات در زمینه قدرت میدان مغناطیسی فوق بالا همراه با فناوری گرادیان فوق سریع دستاوردهای عظیمی در حساسیت، قدرت تفکیک و کنتراست برای تصویربرداری عصبی neuroimaging ایجاد کرده است.در این بررسی یک مرور کلی از مزایا و چالش های فنی انجام مطالعات تصویربرداری عصبی بالینی در حضور قدرت میدان مغناطیسی فوق العاده بالا همراه با تکنولوژی گرادیان فوق سریع ارائه می شود. کاربردهای بالینی نوظهور MRI 7-T و پیشرفتهترین سیستمهای گرادیان مجهز به قدرت گرادیان تا 300 mT/m بررسی میشوند و تأثیر آن و مزایای چنین پیشرفت هایی در MRI آناتومیکال، ساختاری و عملکردی در وضعیتهای مختلف عصب شناسی مورد بحث قرار میگیرد. در نهایت، چشم انداز و مسیرهای آینده برای MRI با میدان فوق العاده بالا( ultrahigh field MRI) تصویربرداری عصبی مورد بررسی قرار می گیرد.
نکات کلیدی
افزایش نسبت سیگنال به نویز و قدرت تقکیک فضایی بالای به دست آمده توسط میدان مغناطیسی فوق العاده بالا (ultrahigh field ) در تصویربرداری رزونانس مغناطیسی (MRI) میتواند برای بهبود توصیف ساختارهای آناتومیکی کوچک و آسیب شناسی ظریف مورداستفاده قرار گیرد. چالش های مرتبط با MRI با میدان فوق العاده بالا شامل آرتیفکت های مرتبط با افزایش اثر پذیرفتاری، غیریکنواختی(ناهمگنی)میدان انتقالی فرکانس رادیویی(RF) انباشت انرژی فرکانس رادیویی افزایش یافته در بافتها است. سیستم های گرادیان با کارایی بالا مجهز به حداکثر دامنه گرادیان و نرخ گردش تحت زاویه 90 درجه بالا (slew rate بالا ) قادر به افزایش قدرت تفکیک فضایی هستند و جمع آوری سیگنال را سریعتر میکنند. محدودیت های تکنیکی سیستم های گرادیانی با عملکرد بالا شامل اثرات بیولوژیکی ناشی از تغییر وضعیت دادن (switching) سریع، میدان های مغناطیسی بزرگ بر روی بدن انسان، که می تواند باعث تحریک اعصاب محیطی شود.
Background
در20 سال گذشته پیشرفت در توسعه فناوری اسکنر تصویربرداری رزونانس مغناطیسی (MRI)با پیشرفت های قابل توجه در قدرت میدان و پیشرفت در طراحی و عملکرد سیم پیچ(کویل) گرادیان همراه بوده است. اسکنرهای MRI بالینی با قدرت میدان مغناطیسی تا T 7 و قدرت گرادیان تا mT/m 80 با یک slew rate 200 T/m/s در حال حاضر به پیشرفته ترین حالت فناوری تصویربرداری برای مطالعات بالینی و تحقیقاتی مغز تبدیل شده است. برای تصویربرداری عصبی، تحقیقات در قدرت میدان مغناطیسی و تکنولوژی گرادیان فوق العاده بالا و فوق العاده سریع منجر به مزایای بسیاری برای قدرت تفکیک بالای آناتومیک، ساختاری و تصویربرداری عملکردی وهمچنین ارائه بینش جدید در پاتوفیزیولوژی بیماری های نورولوژیک شده است .
Ultrahigh field MRI
بررسی مختصر تکنولوژی ها و وضعیت پیشرفت
از آنجایی که اولین تصاویر MRI انسان با میدان فوق العاده بالا در T8 در سال 1998 به دست آمده بود ، MRI با میدان فوق العاده بالا از طریق توسعه و انتشار اسکنرهای T 7 برای تصویربرداری انسان کشش روزافزونی در سراسر جهان به دست آورد . نوید میدان فوق العاده بالاMRI در کنار زدن محدودیت های حساسیت و قدرت تفکیک فضایی، در ابتدا در عرصه پژوهش نشان داده شد و از طریق تجاری سازی اسکنرهای MRI 7-T توسط فروشندگان عمده اسکنر MRI، تشخیص داده شد و اسکنرها توسط سازمان غذا و دارو برای کاربردهای بالینی در سال 2017 تایید و به وسیله ی اسکنرهای MRI با آهنرباهای مغناطیسی 7T Siemens Healthineers و در سال 2020 از طریق اسکنر Electric Healthcare) MRI Signa 7-T (Generalبه اوج خود رسید . بر اساس موفقیت اسکنرهای MRI انسانی 7T و 9.4T فعلی، تلاش های هماهنگ برای توسعه نسل بعدی تولید اسکنرهای MRI میدان بسیار بالا برای استفاده انسان در T 10.5و 11.7T، با قدرت میدان تا T 20 امکان پذیر تلقی می شود و فرصت های جدیدی را برای موارد بی سابقه حساسیت و ویژگی برای تصویربرداری انسان باز می کند.
Challenges and opportunities of imaging at higher field
مزایا و چالش های تصویربرداری در قدرت میدان مغناطیسی ثابت قوی تر( higher field) مستقیماً از وابستگی خواص فیزیکی بافت ها به قدرت میدان مغناطیسی و سایر میدان های مغناطیسی درگیر درشکل گیری تصویر ناشی می شود.
مزیت اصلی افزایش قدرت میدان مغناطیسی برای MRI افزایش حساسیت است. مقیاس سیگنال با قدرت میدان مغناطیسی بیشتر خطی است. در نتیجه افزایش نسبت سیگنال به نویز (SNR) می تواند برای افزایش قدرت تفکیک فضایی و بهبود توصیف ساختارهای آناتومیکی کوچک و آسیب شناسی ظریف استفاده شود.
به عنوان مثال، قدرت تفکیک فضایی تصاویر آناتومیک با وزن T1 می تواند به سطح زیر میلی متری سوق داده شده و تخمین بهتری را از ضخامت بیرونی(قشری) از طریق کاهش اثرات حجم جزئی و بهبود مشاهده زیرزمینه های فضای هیپوکامپ و هسته های آمیگدال را ممکن سازد.
خواص آسایش بافت نیز با قدرت میدان مغناطیسی ، با افزایش مورد انتظار زمان آسایش طولی T1 و کوتاه شدن زمان آسایش عرضی T2 و* T2 در میدان بالاتر تغییر می کند. این تغییرات در خواص آسایش همراه با افزایش SNR برای کاربردهای خاصی سودمند است. به عنوان مثال زمان آسایش طولانی تر T1 نسبت سیگنال به نویز بهتری را برای کاربردهایی مثل زمان پرواز (TOF) آنژیوگرافی تشدید مغناطیسی( MR angiography ) و برچسب گذاری اسپین شریانی( arterial spin labeling )ارائه میدهد. در حالی که زمانهای آسایشT2* کوتاهتر، کنتراست تصویر برای تصویربرداری با وزن (SWI) را بیشتر فراهم میکنند (شکل 1) و برای تشخیص فعال سازی عملکردی وابسته به سطح اکسیژن خون (BOLD) در MRI عملکردی(fMRI) مورد استفاده قرار میگیرد. در واقع، یک مزیت عمده تصویربرداری در میدان بالاتر بهبود تمپورال رزولوشن و SNR و حساسیت بیشتر به همبستگی های زمانی درسیگنال BOLD است که می تواند گره های ناشناخته قبلی در شبکه های عملکردی را اشکار کند .
چالش های مرتبط با MRI میدان فوق العاده بالا عبارتند از : افزایش اعوجاج ناشی از حساسیت درمیدان بالاتر، ناهمگنی میدان انتقال فرکانس رادیویی (RF) ، و افزایش انباشت انرژی RF دربافت ها
با افزایش قدرت میدان، فرکانس تشدید افزایش می یابد و تقریباً 300 مگاهرتز در T 7 است. با در نظر گرفتن خواص دی الکتریک بافت،طول موج میدان انتقال RF درT 7 تقریباً 11 سانتی متر است که کوتاهتر از ابعاد بدن انسان است و منجر به تغییرات قابل توجهی درمیدان انتقال RF به دلیل ایجاد حالت ایستاده امواج میشود. فراتر از افزایش ناهمگنی انتقال، مقدار توان RF ذخیره شده در بافت با قدرت میدان افزایش می یابد ، که منجر به نرخ جذب ویژه بالاتر می شود(SAR). درعمل، MRI بالینی 7T فقط ازکویل های RF فرستنده موضعی استفاده می کند ، که کمیسیون بین المللی الکتروتکنیکال حد آستانه بالاتر از W/kg10 برای SAR موضعی در مقایسه با SAR کل بدن که حد W/kg 2 است توصیه کرده است. استفاده از توالی های MR با قدرت نهشت بالا (به عنوان مثال، اسپین-اکوی سریع (FSE)و بازیابی معکوس inversion-recovery)) در قدرت میدان بالاتر محدود می شود.تغییرات فضایی میدان انتقال RF به دلیل ایستا بودن امواج همچنین می توانند گرمایش موضعی ایجاد کنند. ایمپلنت های فلزی همچنین ممکن است به دلیل جذب RF منجر به گرم شدن شوند، اگرچه بسیاری از مطالعات نشان داده اند که گرمایش ممکن است مشکل کمتری از آنچه در ابتدا پیش بینی می شد و تنها با تغییرات دمای جزئی ناشی از ایمپلنت های کوچک و غیرفعال (مانند گیره های هموستاتیک، گیره های آنوریسم، پروتز دریچه ها، پورت های دسترسی عروقی و استخوانی وایمپلنت های چشمی) باشد .در قدرت میدان بالاتر، جدایی طیفی بین گونه های مختلف شیمیایی افزایش می یابد که منجر به وضوح طیفی spectral) resolution )بالاتر، که برای طیف سنجی (MR Spectroscopy)مفید است ، اما می تواند منجر به آرتیفکت های تصویربرداری بزرگتر به دلیل افزایش جابجایی شیمیایی chemical shift و اثر پذیرفتاریsusceptibility effect شود. آرتیفکتهای پذیرفتاری می توانند در MRI میدان فوق العاده بالا بر کیفیت تصویر تأثیر منفی بگذارند ، به ویژه در تصویربرداری گرادیان اکو . آرتیفکت های ناشی از حساسیت به صورت نتیجه گرادیان های میکروسکوپی یا تغییرات در قدرت میدان مغناطیسی در نزدیکی بافت هایی با حساسیت مغناطیسی مختلف اتفاق بیافتد و منجر به از دست دادن سیگنال و اعوجاج به ویژه در مرز هوا-استخوان و هوا-بافت، باشد و در میدانهای T 7 و بالاتر بیشتر نمایان شود. .از طرف دیگر ، افزایش اثر حساسیت در میدان بالاتر ممکن است برای بهبود اثربخشی تشخیصی مانند افزایش حساسیت به microhemorrhages شود. در نهایت، در حالی که و تمپورال رزولوشن و SNR در میدان بالاتر افزایش می یابد سهم نسبی نویز فیزیولوژیکی که ناشی از عواملی مانند ضربان قلب و حرکت تنفسی است نیز در T 7 در مقایسه با قدرت میدان کمتر افزایش می یابد. استراتژی ها و راهکارهایی برای کاهش اثرات نویز فیزیولوژیکی ضروری است، که به ویژه برای مطالعات fMRI در قدرت میدان بالاتر مهم هستند
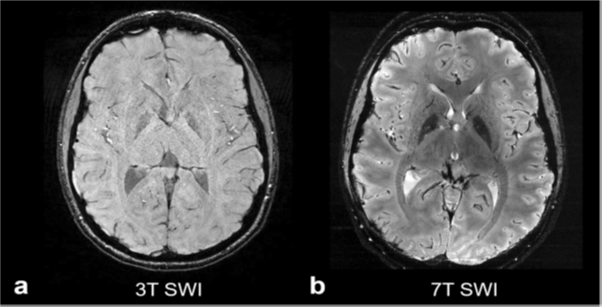
Fig. 1 Comparison of susceptibility-weighted imaging (SWI) using 3-T and 7-T magnetic resonance imaging. Axial SWI images are shown at the level of the basal ganglia in a healthy individual acquired at 3 T (a) and 7 T (b). At higher field strength, the shorter T2* relaxation times result inthe greater SWI sensitivity to magnetic susceptibility differences in the blood vesselsand mineralization in the basal ganglia, particularly in the globus paliduse
Clinical applications of ultrahigh field imaging
قدرت تفکیک فضایی بالا با استفاده از میدان فوق العاده بالا قابل دستیابی است. تصویربرداری با میدان فوق العاده بالا برای مطالعه بیماریهای مختلف استفاده شده است از جمله صرع(epilepsy) ، مولتیپل اسکلروزیس (ms)، تومورهای مغزی، بیماری های عروق مغزی و اختلالات مخرب . بخش های بعدی وضعیت فعلی تحقیق و جهت گیری بالقوه آینده در این زمینه های بالینی را مورد بحث قرار می دهد.
Epilepsy
در بیماران مبتلا به صرع مقاوم به درمان، جراحی ممکن است بهترین شانس را برای رهایی از تشنج ارائه دهد. تصویربرداری عصبی نقش کلیدی در شناسایی صرع کانونی قبل از جراحی صرع دارد. با این حال، تقریبا یک سوم از بیماران مبتلا به صرع کانونی ضایعه قابلت شناسایی در MRI با میدان T 1.5 و T 3 را ندارند. SNR بهبود یافته و قدرت تفکیک فضایی فوق العاده بالا ارائه شده توسط تصویربرداری میدان فوق العاده بالا ممکن است به موضعی سازی مناطق شروع تشنج کریپتوژن کمک کند ،و ممکن است در این بیماران با قدرت میدان معمولی دیده نشده باشد (شکل 2).
در اکثریت بیماران صرعی، عدم تقارن در بیماران بیشتر در همان لوبی است که منطقه مشکوک شروع تشنج است.محققان پیشنهاد کردند که کمیت دور عروقی فضاهای 7 T می توانند نشانگر زیستی تصویربرداری مهمی را برای بررسی اثرات صرع بر مغز وکمک به موضعی سازی ناحیه شروع تشنج در برنامه ریزی جراحی
ارائه دهند.
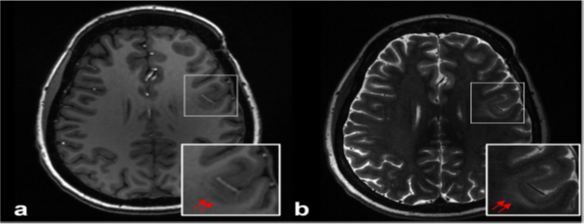
Fig. 2 Anatomical delineation of focal cortical dysplasia at 7 T. Axial T1-weighted (a) and T2-weighted (b) images acquired at 7 T demonstrate blurring of the gray-white matter junction (double arrows), abnormally thick malformed cortex, and an indistinct cortical ribbon in the left inferior frontal gyrus, consistent with focal cortical dysplasia. There is T2 hyperintensity in the subjacent white matter reflecting the white matter component of the dysplasia
مطالعات متعددی این جداسازی عالی را بین مورفولوژی هیپوکامپ و ساختارهای داخلی در T 7 نشان داده اند برای مثال، در تحقیقی بهبود در تشخیص ناهنجاری های هیپوکامپ در 18 بیمار در 7T و ناهنجاری با الکتروانسفالوگرافی و یافته های بالینی در 12 از 18 بیمار مطابق بود . مطالعه دیگری نیز توانست آسیب شناسی در زیرشاخه های ناحیه قشر مغز (CA) با استفاده از MRI میدان فوق العاده بالا را در گروه کوچکی از بیماران با صرع لوب تمپورال نشان دهد که یافته ها با هیستوپاتولوژیک تطابق داشت. ارزیابی ساختار داخلی هیپوکامپ عدم تقارن را در تراکم عروق هم در نئوکورتیکال و هم در مزیال لوب گیجگاهی صرع در هیپوکامپ در مقایسه با افراد سالم، با کاهش نامتقارن تراکم دیواره عروق همان طرف منطقه مشکوک شروع تشنج، نشان داد.با استفاده از تحلیل های حجمی و طیف سنجی رزونانس مغناطیسی درT 7 شناسایی شد که آتروفی ناحیه زیر هیپوکامپ که معمولاً CA3 و غلظت متابولیت های تغییر یافته (به طور عمده سطح گلوتامین کاهش می یابد) در هیپوکامپ بیماران مبتلا به صرع لوب تمپورال تحت تأثیر قرار می دهد. اگرچه حجم و انحراف متابولیت به طور مداوم در هیپوکامپ صرعی، جانبی نیست ، حجم های سابیکولوم پایین تر و غلظت گلوتامین با اختلال عملکرد حافظه کلامی در ارتباط است . با استفاده از حالت استراحت fMRI درتصویربرداری مغناطیسی عملکردی T 7 عدم تقارن شبکه در لوب تمپورال میانی که قادر به تشخیص بین صرع لوب تمپورال بود نشان داده شده است و برای بهبود SNR و قدرت تفکیک بهتر در T 7 که پتانسیل بهبود موضعی سازی را در اختلالات اساسی شبکه مغز در لوب تمپورال بیماران صرعی که کاندید عمل جراحی هستند دارد.
به طور خلاصه، SNR بالاتر و افزایش قدرت تفکیک فضایی توسط MRI با میدان T 7 قابل دستیابی است و نمایش داده میشود تا حساسیت تشخیص ضایعات صرعی را بهبود ببخشد و ممکن است به عنوان هدف ما در شناسایی تغییرات مورفولوژیکی مرتبط با مناطق مشکوک شروع تشنج قرار بگیرد.
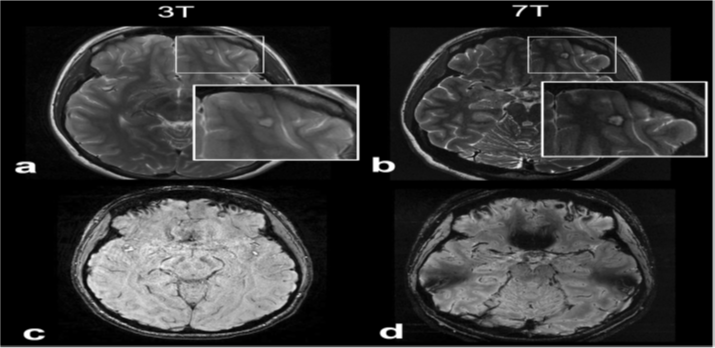
Fig. 3 Cavernous malformation on 3-T and 7-T magnetic resonance imaging. Axial T2-weighted images acquired at 3 T (a) and 7 T (b) show a 6- mm cortical lesion in the left orbitofrontal gyrus with central T2 hyperintensity and peripheral T2 hypointensity. Axial susceptibility-weighted images acquired at 3 T (c) and 7 T (d) show marked susceptibility effect within the rim of the lesion. The 7-T images have higher signal-to-noise ratio and better delineate the lesion compared to the 3-T images. The lesion was resected and found to be a cavernous malformation
Multiple Sclerosis
افزایش حساسیت تشخیص ضایعه و شناسایی بهتر آسیب شناسی ضایعه در 7T نوید ایجاد تمایز بهتر مولتیپل اسکلروزیس (MS) از سایر اختلالات را می دهد. شناسایی یک مرکز ورید داخل ضایعات ماده سفید در MRI، علامت ورید مرکزی (CVS)، به عنوان یک نشانگر زیستی تصویربرداری در تشخیص MS پیشنهاد شده است ، با مطالعات بسیاری نشان می دهد که با وجود CVS دقیقاً MS از تقلیدهای آن متمایز می شود در مطالعه ای روی 7 بیمار با MS و در مجموع 358 ضایعه ماده سفید، Tallantyre و همکارانش نشان دادند که CVS در 87% ضایعات در 7T در مقایسه با 45% ضایعات قابل مشاهده در 3 T با استفاده از توالی های T2*-weightedشناسایی شد. مطالعه بعدی توسط همان گروه نشان داد که در 7T، %80ضایعات در بیماران MS در مقایسه با % 19 ضایعات در بیماران غیر MS و MRI با میدان 7T بر وزن T2* به طور قابل اعتمادی بیمارانMS قطعی از نظر بالینی را از کسانی که MS بالینی ندارند بر اساس درصد ضایعات با CVS متمایز کرد. در مورد یک مطالعه با استفاده از SWI و آماده سازی مغناطیسی بازیابی معکوس تضعیف شده مایع (FLAIR) تصاویر در 7T نشان داده شده است که در آستانه 67٪، ضایعات ماده سفید قبل وریدی به طول 3 میلی متر متلاقی( nonconfluent) بیماران MSدر حال عود کننده از گروه سالم کنترل با حساسیت 94 درصد و ویژگی100٪ قادر به افتراق بودند.
. با وجود این یافته ها، متاآنالیزهای اخیر پیشنهاد کرده اند که در حالی که SNR و نسبت کنتراست به نویز بالاتر اسکنرهایT 7 باعث ترسیم کمی بهتر می شود و تشخیص CVS (نسبت ادغام شده وریدهای مرکزی شناسایی شده در 7T = 0.82)، درسکن 3 T ممکن است در این زمینه کافی باشد (نسبت ادغام شده از وریدهای مرکزی شناسایی شده = 0.74)، در حالی که استفاده از اسکنرهای(1.5T ) از نظر آماری کاهش معنی داری را در تشخیص CVS نشان دادند (نسبت ادغام شده از وریدهای مرکزی شناسایی شده= 0.58)
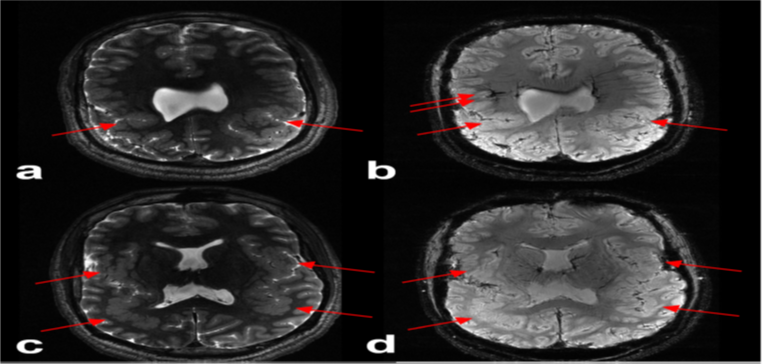
Fig. 4 Sensitivity of 7T magnetic resonance imaging for polymicrogyria. Axial T2-weighted and susceptibility-weighted images at the level of the centrum semiovale (a, b) and lateral ventricles (c, d) demonstrate simplification of the gyral folding pattern involving the perisylvian cortex bilaterally, including the posterior temporal lobes and parietal lobes (red arrows), with thickening of the cortex and nodularity, consistent with polymicrogyria. There is also an abnormally large draining vessel on the right (b, red arrow), which may represent a developmental venous anomaly
فراتر از تشخیص CVS، افزایش قدرت فضایی 7 T تشخیص ضایعات ماده خاکستری قشر مغز را در MS فراهم ساخته است که اغلب در معاینه هیستوپاتولوژیک مشاهده می شود ، اما تشخیص آن در قدرت میدان کمتر به دلیل کاهش کنتراست و قدرت تفکیک فضایی کمتر دشوار است (شکل 5) Cocozza و همکارانش نشان دادند که ضایعات قشر مغز در T 7 در MS قابل شناسایی هستند با استفاده از حجم وزنی T1 سه بعدی (3D) که از نظر زمان بالینی امکان پذیر است و از نظر عملکرد قابل مقایسه بود با آنچه که با استفاده از توالی T2*-weighted به دست آمد. در یک مطالعه طولی با استفاده از یک رویکرد کمی که ترکیبی است از جمع آوری اطلاعات به شکل T2*-weighted gradient-echo در T 7 با تجزیه و تحلیل مبتنی بر سطح، Treaba و همکارانش نشان دادند که ضایعات قشر در MS ترجیحا به صورت داخل قشری و درون شیارهای مغزی توسعه یافته است که تجمع آنها به طور کلی مستقل از ضایعات ماده سفید بود، پاتوژنز این ضایعات نشان می دهد که ناشی از التهاب فرآیندهای مرتبط با مایع مغزی نخاعی(CSF) است. نویسندگان نیز گزارش دادند که تجمع توده ی قشری به طور مستقل پیشرفت ناتوانی عصبی را پیش بینی کرد.
MRI 7-T برای تشخیص MS ضایعات ماده سفید قدرت کمتری نسبت به قشر مغز در بهینه سازی توالی ها برای کاهش محدودیت های ثانویه به SAR بالا و کاهش غیریکنواختی های میدان RF دارند. T2* . ، FLAIR، تصویربرداری انتقال مغناطیسی و مغناطش آماده شده gradient-echo سریع در حال حاضر به عنوان توالی های پیشنهادی برای توصیف ضایعات ماده سفید در 7T توصیه می شود. افزایش قدرت تفکیک فضایی و SNR بالا ام آر آی 7T نیز می تواند در تصویربرداری ضایعات دمیلینه کننده نخاع مفید باشد که به عنوان یک چالش در قدرت میدان پایین تر باقی می ماند. به عنوان مثال، یک مطالعه ی کوچک که تصویربرداری از نخاع بیماران ام اس را در 7T در مقابل 3T مقایسه کرد تجسم بهتری را از آناتومی نخاع و بهبود 50 درصدی در تشخیص ضایعات نخاعی ام اس در 7T در مقایسه با 3T نشان داد. با وجود پتانسیل تئوری مزایای تصویربرداری از نخاع در MS در میدان فوق العاده، چالش های تکنیکی باقی می ماند از جمله فقدان کویل های اختصاصی RF که ممکن است کیفیت تصویرتضعیف شود؛ تغییرات کوچک در پذیرفتاری بافت که در 7T افزایش یافته است و آرتیفکهای حرکتی که به دلیل تنفس، حرکت قلب، بلع و جریان CSF رخ میدهد.
به طور خلاصه، حتی اگر استفاده از MRI با میدان فوق العاده بالا هنوز بخشی از پروتکل های استاندارد تصویربرداری مراقبتی در MS نیست ، امکان تصویربرداری اختصاصی و شناسایی جنبه های مختلف پاتوفیزیولوژی MS را بهتر فراهم کرده است ، در نتیجه بینش جدیدی را نسبت به تنوع بین فردی و سیر تکاملی بیماری ارائه می دهد.
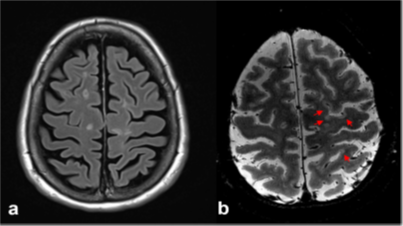
Fig. 5 Cortical lesions in multiple sclerosis on 3-T and 7-T magnetic resonance imaging. Axial fluid-attenuated inversion-recovery (FLAIR) image acquired at 3 T (a) and axial T2*-weighted image acquired at 7 T (b). The 7-T image shows many more cortical lesions (red arrows), which are not visible on the axial FLAIR (a) or T2-weighted image (not shown) at 3 T, due to a combination of increased contrast and spatial resolution at 7 T
Brain tumors
. چندین مطالعه پیشنهاد می دهد که ام آر آی 7T می تواند اطلاعات بهتری در مورد میکروواسکولاریته و نکروز از MRIبا میدان 1.5T و 3T داشته باشد و می تواند طبقه بندی اولیه بیماران مبتلا به گلیوما را بهبود بخشد(شکل 6)، (مطابق با با طرح های درجه بندی اخیر سازمان جهانی بهداشت) میکروواسکولاریته بالای تومور در گلیوماهای درجه بالا در مقایسه با ضایعات درجه پایین با استفاده ازسکانس SWIو 7 Tبهتر نشان داده میشود ، یک تکنیک واریانس محلی تصویر برای کمی سازی ساختارهای میکروواسکولار SWI کم شدت درT 7 قادر به افتراق نفوذ پذیری گلیوم بر اساس درجه تومور و ایزوسیترات دهیدروژناز(IDH) وضعیت جهش است .
اخیراً از آنژیوگرافی TOF MR در 7T برای مشخص کردن عروق داخل تومور در یک نمونه کوچک 12 بیمار مبتلا به گلیوم استفاده شده است که نتایج خوبی به دنبال داشته است: مزایای آنژیوگرافی TOF در 7T در مقایسه با قدرت میدان پایین تر (افزایش SNR، زمان آسایش T1 طولانی تر افزایش کنتراست رگ-بافت و افزایش شدیدعروق شریانی) نشان می دهد که ممکن است یک روش غیرتهاجمی مفید برای درجه بندی گلیوما از گلیوماهای درجه بالاتر که تمایل به افزایش رگزایی دارند، باشد. علاوه بر این، تصویربرداری عروقی 7T برای مطالعه تغییرات میکروواسکولار طولی گلیوما پس از درمان ضد رگ زایی، با نقش بالقوه در نظارت غیر تهاجمی پاسخ درمانی ضد رگ زایی در بیماران مبتلا به تومورهای تهاجمی مغزی به کار گرفته شده است.
تصاویر FLAIR با قدرت تفکیک بالا در 7T با سکانس FLAIR بالینی در 3T در بیماران مبتلا به گلیوبلاستوما قبل از برنامه ریزی( planning )رادیوتراپی مقایسه شدند و SNR به طور قابل توجهی بالاتر در ماده سفید و کنتراست بهتر بین ماده خاکستری و سفید در مقایسه با توالی های بالینی FLAIR به همراه داشت محققین پیشنهاد کردند که دید بهتر مرزهای آناتومیکی توسط کنتراست ماده خاکستری و ماده سفید بهبود یافته در سکانس FLAIR در 7T فراهم می شود و میتوان در بهبود ترسیم ساختارهای مغزی در معرض خطر در طول برنامه ریزی درمان به کار گرفت. یک مطالعه اخیر نشان داد که در بیماران گلیوما ، سدیم (23Na) در MRI با میدان 7T با وضعیت جهش ایزوسیترات دهیدروژناز (IDH) با کاربرد بالقوه در بیوپسی با هدایت تصویر، جراحی و رادیوتراپی همبستگی دارد.نویسندگان همچنین کاهش پی در پی غلظت 23 Na از مناطق نکروز مرکزی به ظاهر طبیعی ماده سفید که نشان دهنده یک همبستگی با نفوذ تومور است را گزارش کردند. طیف سنجی تشدید مغناطیسی (MRS) در قدرت میدان بالاتر SNR و پراکندگی طیفی را بهبود می بخشد، منجر به بهبود حساسیت و ویژگی، به ترتیب، به گونه های شیمیایی و متابولیت های مختلف میشود. MRSپتانسیل بهبود تشخیص متابولیت ها را برای شناسایی تومور دارد ؛ با این حال، چالش های تکنیکی افزایش SAR، ناهمگنی میدان مغناطیسی، زمان آسایش سریع T2* می تواند محدودیت هایی را بر روی کسب داده های MRS در 7Tتحمیل کند با وجود این محدودیت ها، تحقیقات قبلی در استفاده از توالی MRS اسپین-اکوی کوتاه اکو 7T قادر به نشان دادن برای تشخیص تفاوت های مشخصه در مناطق تومور در مقابل ظاهر طبیعی مغز و با موفقیت در تمایز قائل شدن بین متابولیت های کوتاه اکو، به ویژه گلوتامات و گلوتامین، هر چند با Spatial Resolution کمتر در قدرت میدان 3T و پایین تر این تمایز گمراه کننده باقی می ماند . دهه گذشته رویکردهای مختلف جمع آوری اطلاعات MRS را برای جبران برخی از چالش های تصویربرداری میدان فوق العاده بالا دیده است . در تحقیقی با موفقیت تفاوت متابولیک بین نواحی تومور و بافت های اطراف تومور را برای متابولیت های متعدد با استفاده از یک روش MRS سه بعدی تمام مغز سریع با قدرت تفکیک بالا در 23 بیمار با تایید بافت شناسی گلیوما درجه بالا نشان داده شد اگرچه 2-هیدروکسی گلوتارات (2HG) در این مطالعه، به طور رضایت بخشی تعیین نشده است سایر مطالعات، تشخیص 2HG در میدان فوق العاده بالا را نشان داده اند. در تحقیق دیگری 2HG با استفاده از MRS در میدانT 9.4 نشان داده شد. با این حال، ارزیابی اضافی مطالعات با استفاده از حجم نمونه بزرگتر برای کمی سازی 2HG و سایر متابولیت های سرطانی در میدان بسیار بالا مورد نیاز است. تصویربرداری انتقال اشباع تبادل شیمیایی (CEST)، یک تکنیک کنتراست جدید است که می تواند غلظت کم متابولیت هایی که با حساسیت بالاتر از MRS استفاده شده است را در هر دو قدرت میدان بالینی و فوق العاده بالا برای تمایز گلیوما تشخیص دهد .
به طور خلاصه، MRI میدان فوق العاده بالا تشخیص متاستازهای کوچک، تعیین وسعت تومور،توصیف ریزمحیط داخل توموری، و تشخیص اثرات پس از درمان در هنگام مقایسه به ام آر آی قدرتی معمولی را بهبود می بخشد با این حال، چالش های فنی مربوط به MRS و تکنیک های جدید CEST باقی مانده است و تحقیقات تکمیلی را ایجاب می کند.
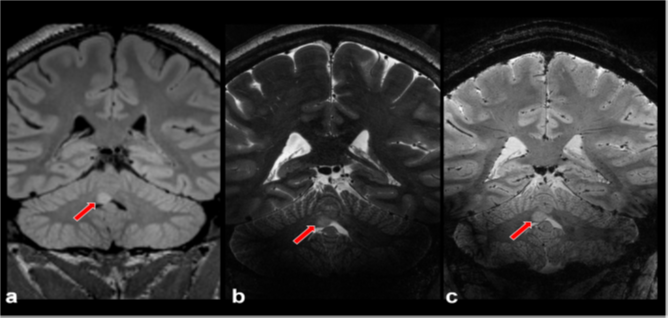
Fig. 6 Hamartoma identified on 3-T magnetic resonance imaging and further characterized at 7 T. Coronal T2-weighted fluid-attenuated inversion-recovery image at 3 T (a) demonstrates a hyperintense mass (red arrows) in the right cerebellar vermis. Coronal T2-weighted (b) and coronal susceptibility-weighted image (c) obtained at 7T show no evidence of microvascularity within the lesion
Neurodegenerative disorders
مطالعات درT 7 در زمینه اختلالات عصبی عمدتا بر روی زوال عقل از جمله بیماری آلزایمر (AD) و زوال عقل عروقی و بیماری پارکینسون (PD) تمرکز کرده اند. اگرچه هیپرفسفریله شده تاو و آمیلوئید بتا به عنوان واسطه های کلیدی پاتوژنز AD در نظر گرفته می شوند ، تعداد فزاینده ای از مطالعات نشان می دهد که متابولیسم آهن تغییر یافته نیز نقش مهمی ایفا می کند. MRI با وزن T2 در 7T پس از مرگ بر روی قشر پیشانی بیماران مبتلا به AD با شروع زودرس و دیررس و همچنین کنترل اختلال شدید در لمینیت قشر مغز بیماران AD نشان داده شده است ، که تجمع میلین و آهن با تغییرات در قشر مغز مرتبط است . مطالعه بعدی توسط همان گروه پس از مرگ در لوب تمپورال داخلی بیماران مبتلا به AD و شاهد ارزیابی شد و همچنین تنوع بیشتر در لمینیت قشر مرئی لمینیت در بیماران مرحله پیشرفته AD نشان داد قشر مغز به شدت تحریف شده ؛ تغییرات ظاهری قابل مشاهده ورقه ورقه شدن قشر با انتشار تغییرات آهن و انباشت آهن همراه بود. مجموعه ای از مطالعات از MRI 7-T برای ترسیم الگوی آتروفی زیرساختارهای مختلف هیپوکامپ دربیماران AD با مفاهیمی برای درک نوروپاتوژنز دخیل در از دست دادن حافظه در این بیماران استفاده کرده اند . با یک توپوگرافی می توان ارتباط بین درجه بالایی از اتساع فضای اطراف عروقی juxtacortical در خونریزیهای ریز مجاورت قشر مغز در اختلال شناختی خفیف فراموشی و بیماران اولیه AD که ممکن است به دلیل اختلال در زهکشی مایع بینابینی مربوط به رسوب آمیلوئید دور عروقی باشد را نشان داد. نویسندگان پیشنهاد کردند که فضاهای اطراف عروقی گشاد شده در میدان فوق العاده بالا ممکن است به عنوان نشانگر آنژیوپاتی تصویربرداری عصبی آمیلوئید مغزی غیر مستقیم دربیماران AD عمل کند. تحریک عمقی مغز (DBS) هسته های هدف مانند هسته زیر تالاموس،قسمت داخلی globus pallidus ، و هسته بطنی داخلی میانی تالاموس به طور گسترده برای جراحی و درمان بیماران مبتلا به PD که در آن یک الکترود برای تحریک اجزای موتور استفاده میشود در حالی که از اجزای ارتباطی و اجزای لیمبیک اجتناب میشود. کنتراست تصویری بهبود یافته، قدرت تفکیک و SNR درT 7 امکان تجسم بهبود یافته هسته های هدف DBS را در مقایسه با اسکنرهای استانداردT.5-T یا 3T فراهم می کند. در تحقیقات دیگری از دسته بندی مبتنی بر tractography در 7T در بیماران PD قبل از جراحی DBS برای تقسیم قلمروهای کاربردی قسمت داخلی globus pallidusبه اجزای حرکتی، ارتباطی و لیمبیک شناسایی و استفاده کردند که به صورت شیوه تکرارپذیر سازماندهی شده بودند. به طور مشابه، با استفاده از پروتکل بسته بندی مبتنی بر یک اتصال ساختاری ، هسته ساب تالاموس
اتصالات به موتور، لیمبیک و نواحی قشر وابسته برای ترسیم مولفه های فرعی هسته در بیماران مبتلا به PD ایدیوپاتیک، استفاده شد و نقش تصویربرداری میدان فوق العاده بالا را در تسهیل برنامه ریزی فردی عمیق جراحی تحریک مغز بیشتر تقویت می کند.
تفاوت در الگوهای آناتومیکی ماده سیاه (substantia nigra) بین بیماران PD و داوطلبان سالم در MRI با میدان T 7Tنیز استفاده می کنند که می تواند امکان تشخیص زودهنگام بیماری را فراهم می کند. اخیرا مطالعه تغییرات قابل توجهی را در مورفولوژی هسته ساب تالاموس (حجم کمتر) و ریزساختاری سازماندهی (ناهمسانگردی کسری پایین) در بیماران بزرگسال با PD خفیف تا متوسط در مقایسه با سالمندان سالم نشان داد ، که تغییرات نورودژنراتیو در PD فراتر از قسمت ماده سیاه فشرده گسترش می یابد تا درگیر مسیرهای عقده های قاعده ای(Basal Gangalia) فوق مستقیم و غیر مستقیم شود. در نهایت،از تصویربرداری میدان فوق العاده بالا برای شناسایی تغییرات درsubfield های هیپوکامپ در بیماران مبتلا به PD استفاده شده است و مکانیسم های عصبی آناتومیکی زمینه ای اپیزودیک اختلالات حافظه که در PD دیده می شود به درک ما می افزاید.
به طور خلاصه، قدرت تفکیک تصویر در MRI با میدان 7T افزایش یافت و تجسم ساختارهای کوچک پاتوفیزیولوژی تخریب کننده عصبی از جمله قشر مغز لایه ها، زیر فیلدهای هیپوکامپ، هسته های ساقه مغز، پلاک ها، و میکروبلیدها مورد علاقه را امکان پذیر می کند. MRI-7T برای شناسایی نشانگرهای زیستی بیماری در هر دو بیماری AD و PD با موفقیت به کار گرفته شده است و ممکن است مکمل قدرتمندی برای سایر روش های تصویربرداری غیرتهاجمی در ارزیابی های زوال عقل باشد.
.
Cerebrovascular diseases
MRI حساس ترین تکنیک تصویربرداری تشخیص انفارکتوس حاد است و بدین منظور پروتکل هایی تصویربرداری بالینی سکته مغزی برای تصویربرداری انفارکتوس مزمن تحت حاد در T 7 طراحی شده اند. به استثنای تصویربرداری بر وزن انتشار(DWI) به عنوان بخشی از پروتکل استفاده از آن در کار بالینی فعلی برای ارزیابی بیماران سکته مغزی حاد پیشگیری میشود. با وجود این، SNR بالا ، قدرت تفکیک فضایی بالا و CNR بالا ارائه شده توسط MRI میدان فوق العاده بالا می تواند برای ارزیابی ضایعات عروق مغزی کوچک استفاده شود (مانند انفارکت های ریز قشر مغز) و عروق در مقیاس زیر میلیمتری، در نتیجه توصیف بهتر بیماریهای عروق مغزی از جمله سکته مغزی با استفاده از T 7 در مقایسه با قدرت میدان کمتر را اجازه میدهد. آنژیوگرافی MR در7T با موفقیت در تغییرات انسدادی عروق کوچک مانند لنتیکولستریت عروق در سکته های حاد و مزمن استفاده شده است ؛ تصویربرداری از این رگ ها با روش های مرسوم دشوار است علاوه بر این، زمانی که تصاویر بیماران با سکته مغزی تحت حاد و مزمن در T 7 و T 3 مقایسه شد ، قدرت تفکیک فضایی بالاتر اسکنرهای T 7 مقایسه ویژگیهای ظریف مورفولوژی انفارکتوس به تصاویر MR با میدان پایین را نشان داد.آترواسکلروز داخل جمجمه ای یک فاکتور ریسک اصلی سکته مغزی ایسکمیک است. تحقیقات از مزایای تصویربرداری میدان فوق العاده بالا فراتر از به تصویر کشیدن لومن از عروق داخل جمجمه ای با کالیبر کوچکتر، برای ارزیابی به طور مستقیم دیواره عروق داخل جمجمه استفاده کرده است .ام آر آی در 7T نسبت به MRI 3Tدر خصوصیات دیواره عروق برتر و تجسم کلاهک فیبری و هسته لیپیدی در پلاک های آترواسکلروتیک در بیماران مبتلا به بیماری آترواسکلروتیک داخل جمجمه برتر بود، و نقش بالقوه MRI 7Tدر طبقه بندی ریسک آترواسکلروز را در داخل جمجمه پیشنهاد می کند. مطالعه دیگری که در شرایط آزمایشگاهی سونوگرافی داخل عروقی و یافته های MRI 7T با بافت شناسی مرتبط است نتیجه گرفت که MRI 7T یک روش قابل اعتماد برای تشخیص بار آترواسکلروتیک شریان ها در داخل جمجمه است.
افزایش SNR، قدرت تفکیک فضایی بالاتر و سرکوب بهتر مایع دیده شده در 7T نیرویی اعمال کرده است تا بیماران دارای آنوریسم که در معرض خطر بالایی از پارگی پلاک آترواسکلروتیک هستند را ارزیابی کرده و پارگی و مشخصه مورفولوژی انفارکتوس را پیش بینی کنید. محقیقن با استفاده از T1- تقویت شده (Enhanced) با گادولینیوم مغناطش وزنی آماده توالی گرادیان اکوی سریع (MPRAGE) در 7T برای توصیف آنوریسم ریزساختارهای دیواری که مسئول افزایش گادولینیوم هستند استفاده میشود و در قدرت میدان کمتر دیده نمی شود. افزایش جزئی یا کامل دیواره داخلی با نئوواسکولاریزاسیون از لایه دیوار داخلی و همچنین مجاور ترومبوز و افزایش جزئی یا کامل دیواره خارجی مرتبط است را می توان با تشکیل vasa vasorum در لایه دیواره خارجی آنوریسم توصیف شود. نویسندگان نتیجه گرفتند که افزایش دو لبه دیده شده در 7T با ادم پری فوکال همبستگی دارد و یافته های بافت شناسی دیواره حکایت از بی ثباتی دارد. در مطالعه دیگری که 7Tو 1.5T ، نشان داده شد که تشخیص و شناسایی پارگی آنوریسم در 7T بهتر استWredeو همکاران نشان دادند که تصاویر با آنژیوگرافی تفریق دیجیتال TOF MR با میدان 7Tبا استاندارد های طلایی فعلی قابل مقایسه بودند.
به طور خلاصه، تصویربرداری دیواره عروق میدان فوق العاده بالا در ارزیابی تشخیص، تمایز بهتر فرآیندهای زمینه ای بیماری عروق مغزی ممکن است زودتر امکان پذیر باشد و ارائه اطلاعات ارزشمند در مدیریت بیماری عروق داخل جمجمه ای فراهم کند با این حال،محرومیت محدودیت های DWI استفاده از MRI-7Tرا در ارزیابی بیماران سکته مغزی حاد در این زمان محدود می کند.
Ultra-high and ultrafast gradient technology
بررسی مختصر تکنولوژی و مدرن بودن
سیستم گرادیان به عنوان یکی از اجزای اصلی اسکنر، است که نقش کلیدی در تولید تصویر MR با انتخاب فضایی و encoding تصویر ایفا می کند عملکرد ویژگی های سیستم گرادیان با حداکثر دامنه گرادیان، پارامتری شده است که اندازه گیری می شود بر حسب mT/m، وrate slew، که توصیف می کند گرادیان با چه سرعتی می تواند به دامنه دلخواه در یک مقدار زمان معین (T/m/s) دست یابد. گرادیان میدان مغناطیسی تأثیر فوق العاده ای بر کیفیت کلی تصویر اکتسابی دارند ، هدفی که تمرکز فزاینده ای از سوی تولید کنندگان عمده اسکنر که در تلاش برای بهبود کیفیت تصویر و encoding سریعتر تصویر هستند ،پیدا کرده است .تلاش های مهندسی قابل توجهی در 30 سال گذشته برای به حداکثر رساندن عملکرد سیستم های گرادیانی برای استفاده بالینی انجام شده است جدیدترین نسل اسکنرهای تجاری مانند SIEMENS Prisma، GE Premier و Philips Achieva 3T X-series (سیستم گرادیان دوگانه Quasar) است سیستم های گرادیان دارای بدنه یکپارچه با حداکثر دامنه گرادیان mT/m 80و به ترتیب حداکثر سرعت حرکت 200، 100 T/m/s. برای کاربردهایی مانند diffusion MRI ، کویل های گرادیان قادر به تولید میدان های گرادیان با دامنه های بالا زمان مورد نیاز برای رمزگذاری(encoding) انتشار و به طور قابل توجهی کاهش می دهد و چنین اندازهگیریهایی با کاهش فروپاشی سیگنال ناشی از آسایش T2 بهبود SNRرا باعث میشود. کویل های گرادیان سر با قطر کمتر یک جایگزین مناسب برای دستیابی به حداکثر دامنه گرادیان حتی بالاتر در مقایسه با گرادیان کل بدن هستند و طرح مورد علاقه برای ادغام کویل ها به سیستم های MRI 3-T با استفاده از گرادیان های تقویت کننده قدرت در دسترس بالینی باقی مانده اند. به عنوان مثال، MAGNUS (شیب آناتومی ریز ساختار برای تصویربرداری عصبی با اسکن فوق سریع)
( (Microstructure Anatomy Gradient for Neuroimaging with Ultrafast Scanningکویل گرادیان سر mT/m 200 ارائه می دهد با حداکثر دامنه گرادیان و slew rate بالای T/m/s 500 در هر محور در قطر سوراخ 37 سانتی متری با استفاده از تقویت کننده های کم توان (620 A/1500 V) نسبت به آن ها در اسکنر Connectom استفاده شده است.
Challenges and opportunities of imaging with higher performance gradient systems
سیستم های گرادیان عملکرد بالاتر مجهز به حداکثر دامنه گرادیان و نرخ slew بالاتر که افزایش قدرت تفکیک فضایی و اکتساب سریعتر را مقدور می سازد. برای دستیابی به قدرت تفکیک فضایی بالاتر، گرادیان قوی تر مورد نیاز است، توجه داشته باشید که حداکثر مساحت زیر یک پالس کدگذاری گرادیان بالاترین رزولوشن فضایی قابل دستیابی را تعیین می کند. این را می توان با استفاده از قدرت میدان پایین تر با طولانی کردن کدگذاری گرادیان پالس ها بدون افزایش دامنه آنها به دست آورد ؛ متاسفانه این رویکرد منجر به از دست دادن SNR به دلیل کاهش سیگنال مرتبط در طول دوره بازخوانی تصویر T2 می شود.. برای اینکه زمان خواندن تصویر را بدون کاهش رزولوشن کوتاه کنید، دامنه گرادیان باید افزایش یابد، و زمان را برای رسیدن به دامنه گرادیان مورد نظر باید به حداقل رساند. بنابراین سیستم های گرادیان با کارایی بالا برای به حداکثر رساندن دامنه گرادیان و slew rate با محدودیت های تکنیکی و بیولوژیکی کوتاه طراحی شده است. کوتاه شدگی پالس های گرادیان در حین بازخوانی تصویر باید با دقت انجام شوند و در برابر کاهش SNR تصویر فراتر از یک حد قابل قبول آن متعادل باشد، زیرا SNR با جذر پهنای باند، که توسط دامنه گرادیان تنظیم میشود رابطه معکوس دارد. محدودیت های تکنیکی شامل چالش های مهندسی برای دستیابی به یک گرادیان میدان مغناطیسی خطی فضایی ، حذف گرما از گویل های گرادیان، و راندمان و توان مورد نیاز کویل های گرادیان می شود در حالی که این چالش های فنی تا حد زیادی مورد توجه دوران مدرن، از جمله پیشرفت در گرادیان و تکنولوژی shim قرار گرفته است. عامل محدود کننده اصلی عملکرد سیم پیچ گرادیان اثر بیولوژیکی سوئیچینگ سریع میدان های مغناطیسی بزرگ بر روی بدن انسان است. تحریک پیرامونی عصبی (PNS) اگر محصول نرخ سوئیچینگ گرادیان و قدرت تولید میدان های الکتریکی به اندازه کافی بزرگ باشند می تواند باعث شلیک عصبی شوند، که می تواند ناراحت کننده و بالقوه دردناک باشد. به خاطر چنین نگرانی های ایمنی، تحریک اعصاب محیطی به شدت در MRI تنظیم می شود. اختلاط آناتومیک مدل های اعصاب محیطی نسبت به الکترومغناطیسی و شبیه سازی نورودینامیک PNS وعده پیش بینی دقیق تر آستانه های PNS می دهد و ممکن است طراحی سایز سیم پیچ های گرادیان PNS را به حداقل برساند. کویلهای سر کوچکتر فقط قسمت نواحی سر و گردن را پوشش می دهد و مسیرهایی در قفسه سینه و پشت که به ویژه به تحریک مستعد هستند القای جریان را از بین می برند ، و ارائه استراتژی دیگری برای کاهش PNS در تصویربرداری مغز پیشنهاد میشود.
Clinical applications of ultrahigh gradient technology Anatomic MRI
گرادیانهای های قوی تر و سریع تر با قادرساختن بازخوانی کارآمدتر تصویر، همراه با کاهش زمان اکو و زمان تکرار بسته به کنتراست تصویر مورد علاقه به تصویربرداری آناتومیک کمک می کند. پس از آن می توان از زمان کسب اطلاعات کوتاه شده برای افزایش قدرت تفکیک فضایی و یا SNR از طریق میانگین گیری سیگنال در یک زمان اسکن کلی مشابه استفاده کرد به عنوان مثال، با استفاده از سیستم گرادیان کل بدن Connectome با حداکثر قدرت شیب mT/m 300 و سرعت حرکت T/m/s 200 ، و در مقایسه با سیستم گرادیان کل بدن با قدرت گرادیان 60 mT/m و حداکثر سرعت حرکت 200 T/m/s و ، بهبود در آناتومیک تصویربرداری شامل 25% کاهش در زمان تکرار و 50٪ کاهش در زمان اکو است برای توالی 3 بعدی MPRAGE با وزن T1 به دلیل echo spasingکوتاهتر ، که به کاهش تقریباً 25٪ در زمان کسب اطلاعات منجر میشود. فشار مداوم برای زمان اسکن کوتاه تر منجر به توسعه طرح های نمونه برداری فضای k کارآمدتر برای تصویربرداری دو بعدی و سه بعدی که از مزایای گرادیان عملکردی بهتری بهره می برند میشود. encodingفضای k اسپیرال برای استفاده کارآمد از سخت افزار سیستم گرادیان و دستیابی به زمان های اکو فوق کوتاه و کاربردهای تصویربرداری سریع به صورت بلادرنگ استفاده شده است . به عنوان مثال دیگری ، تاشدگی (aliasing)کنترل شده با امواج در تصویربرداری موازی(CAIPI) یک تکنیک تصویربرداری موازی سه بعدی است که از الگوی کنترل شده مدولاسیون گرادیان در فاز و دستورالعمل های رمزگذاری پارتیشن برای ایجاد جابجایی CAIPI دو بعدی بین پارتیشن ها و انتشار وکسل در هر سه ابعاد با استفاده از گرادیان های سینوسی استفاده میکند. Wave CAIPI از اطلاعات حساسیت گرادیان سه بعدی هنگام استفاده از کویل های آرایه با تعداد کانال بالا با فاکتورهای شتاب بالا بهره کامل می برد و جریمه فاکتور g در انواع کنتراست ها آرتیفکت های ناچیز رافراهم می کند. به طور کلی، دامنه گرادیان بالاتر و پهنای باند کمتر انتشار وکسل بیشتر تولید می کند ، slew rate بیشتر امکان افزایش تعداد سیکل های سینوسی را در هر دورهencoding، فراهم می کند که مقدارآرتیفکت در تصاویر به دست آمده را کاهش می دهد Wave-CAIPI از مزیت از قدرت گرادیان بالاتر و slew rate سریع برای قادر ساختن قدرت تفکیک بالاتر و تصویربرداری آناتومیک سریعتر استفاده می کند. عملکرد تشخیصی که Wave-CAIPI دارد نشان داده شده است که معادل توالی های آناتومیک استاندارد سه بعدی به دست آمده با تصویربرداری echo planar معمولی همراه انواع کنتراست ها با کاهش آرتیفکت های زمان اسکن و حرکت است.
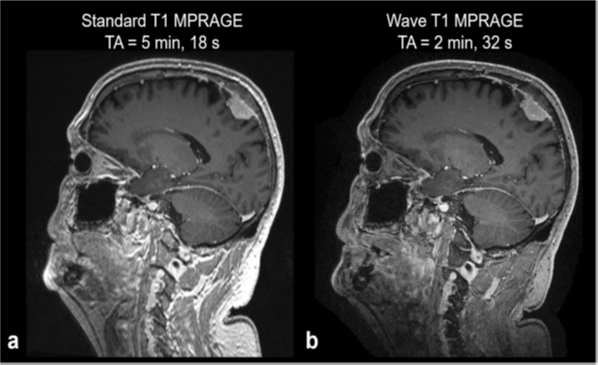
Fig. 7 Comparison of post-contrast three-dimensional T1-weighted magnetization prepared rapid acquisition gradient recalled echo (MPRAGE) images acquired with conventional parallel imaging and wave-controlled aliasing in parallel imaging (CAIPI) encoding demonstrating a meningioma. Standard (a) and Wave-CAIPI (b) T1-weighted MPRAGE images show equivalent visualization of the dural-based enhancing mass along the parietal convexity. Both images were acquired on a 3-T Siemens Prisma MRI scanner equipped with 80 mT/m maximum gradient strength and 200 T/m/s maximum slew rate. The Wave-CAIPI sequence was more than twice as fast as the standard sequence (acquisition time =2 min, 32 s for Wave-CAIPI compared to 5 min, 18 s for the standard sequence)
Diffusion MRI
سیستم های گرادیان با کارایی بالا مجهز به حداکثر دامنه گرادیان بزرگ به ویژه برای MRI diffusion سودمند است ، زیرا آنها کاراییencoding انتشار را افزایش می دهند. استفاده از گرادیان های قوی تر، در ناحیه گرادیان کدگذاری انتشار داده شده که باید در آن زمان کمتر و به طور موثر کل دوره و زمان اکو به دست آید، کدگذاری انتشار را کوتاه می کند ، در نتیجه سیگنال کمتری از آسایش T2 از دست می رود. فراتر از افزایش SNR، دامنه های گرادیان بزرگتر کدگذاری انتشار قوی تر با انتشار موثر کوتاه تر را امکان پذیر می کند ، که حساسیت اندازه گیریMRI انتشار را به ساختارهای میکروسکوپی روی مقیاس میکرون بهبود می بخشد و قدرت تفکیک ساختارهای ریز مانند الیاف متقاطع برای تراکتوگرافی انتشار را بهبود می بخشد. در دسترس بودن عملکرد بالا اختصاصی کویل های گرادیان با حداکثر دامنه گرادیان بزرگ نوع های جدیدی از اندازهگیریهای MRI انتشار را امکانپذیر میکند که در مغز انسان زنده اجرا شود و پروب حساس تری از ریزساختار ماده سفید در بیماری های عصبی مختلف فراهم می کند. دامنه گرادیان بالا برای تخمین خواص ریزساختاری مانند چگالی نوریت و پراکندگی جهت گیری ، قطر آکسون و ابعاد فضای خارج سلولی بافت مفید است ، که خواص بیشتری را به تغییرات ریزساختار بافت نسبت به تصویربرداری تانسور انتشار ارائه می دهند. تخمین قطر آکسون از جمله خواص ریزساختاری بافت است که می تواند با استفاده از MRI انتشار، اندازه گیری شود برای حساس کردن به انتشار سیگنال MRI به انتشار آب به دامنه های گرادیان بالا نیاز دارد. نقشه برداری ضخامت آکسون با استفاده از گرادیان بالا MRI انتشار برای مطالعه از تغییرات در ساختار آکسون و چگالی بسته بندی در MS و نقشه برداری مغز سالخورده استفاده شده است قطر آکسون در جسم پینه ای بیماران MS عود کننده- فروکش کننده و پیشرونده ، قطر آکسون افزایش و چگالی آکسون در ضایعات کاهش و ظاهر طبیعی ماده سفید مطابق با یافته ها در هیستوپاتولوژی است، که نشان دهنده کاهش چگالی آکسون و افزایش کلی در قطر آکسون در پس از مرگ بافت MS است. افزایش مشاهده شده در قطر آکسون که توسط MRI انتشار با گرادیان بالا اندازه گیری می شود همچنین پیش بینی کننده قوی ناتوانی و اختلال عملکرد شناختی است ، به ویژه در تست های بین نیمکره ای سرعت پردازش و حافظه کاری که جسم پینه ای به عنوان فیبر اصلی ماده سفید که دستگاه واسطه این فرآیندها است بر آن تکیه دارند. کاربرد نقشه برداری از قطر آکسون با پیشرفت سن افزایش قابل توجهی در قطر آکسون در ماده سفید قدامی با تغییرات بیشتر در جنس جسم پینه و پنس مینور به پیری مغز کشف شده است. این تغییرات در قطر آکسون با منطقه ای که قبلا گزارش شده است سازگار است در ناهمسانگردی کسری در داخل ماده سفید پیشانی کاهش می یابد و موازی ناحیه جسم پینه ای و حجم ماده خاکستری منطقه ای با بالارفتن سن کاهش می یابد. در دسترس بودن گرادیان های فوق قوی برای MRI انتشار ترجمه کدگذاری انتشار جدید را فعال کرده است ،که شامل پارادایم هایی برای بررسی ریزساختار بافت مغز در بیماران، از جمله شکل موج رمزگذاری دو برابر انتشار گرادیان نوسانی و مسیر تصویربرداری فضایی q است. یک مطالعه اخیر کدگذاری انتشار ایزوتروپیک را با گرادیان انتشار فوق قوی برای دستیابی به وزن انتشار بالا ترکیب کرد در محدودیت های بالا، فضا های کروی محدود شده ،(به اصطلاح dot compartment) در ماده خاکستری مخچه در حالی که سیگنال ناشی از آب غیرایزوتزوپیک در داخل آکسون ها سرکوب می شود. با به دست آوردن ویژگی بیشتر برای آثارسلولی در مخچه، رمزگذاری تانسور کروی با قدرت گرادیان بالا انجام شده ممکن است باعث شود شناسایی زودتر از دست دادن ماده خاکستری مخچه در بیماران با آتاکسی های ارثی مانند آتاکسی نوع 2 نخاعی-مخچه ای که به طور انتخابی بر روی گرانول و سلول های پورکنژ اثر میگذارد. توانایی پروب در انتشار میکروسکوپی ناهمسانگردی در تومورهای مغزی با استفاده از تصویربرداری مسیر فضایی q ممکن است باعث تمایز تومورهای مغزی مانند مننژیوگلیوما از تومورهای گلیوما درجه بالا بر اساس مورفولوژی و ترکیب سلولی آنها شود.
نتایج مطالعات تحقیقات بالینی، پتانسیل MRI انتشار با گرادیان بالا برای کشف تغییرات در ریزساختارهای آکسونی و سلولی و ایجاد انگیزه توسعه مداوم، کاربرد و پخش فناوری با گرادیان بالا برای استفاده در اسکنرهای MRI انسانی موجود در بازار را نشان می دهد.
Functional MRI
قدرت گرادیان بالاتر و slew rate سریعتر توسعه و استفاده از acquisition های fMRI شتاب داده شده با قدرت تفکیک فضایی بالا را تسهیل می کند. گرادیان بالاتر و slew rate های سریع تر به طور مستقیم به بهتر شدن کیفیت تصویر برای تصویربرداری اکو پلانار منجر مشود، workhorse بازخوانی تصویر MR عملکردی، با افزایش SNR، کاهش اعوجاج، قدرت تفکیک بالاتر در صفحه و برش های نازک تر را مقدور میسازد. فراتر از مزایای کیفیت تصویر ، slew rate سریع در دسترس سیستم های گرادیان با عملکرد بالا وعده افزایش کارایی acquisition را می دهند و نمونه برداری متراکم از تکامل سیگنال T2 و T2* برای نقشه برداری کمی سریع سیگنال BOLD ناشی از عروق کوچک و میکرو را فراهم می آورند. کسب دادههای fMRI با قدرت تفکیک زمانی ویا مکانی بالاتر قول می دهد اطلاعات جدیدی در مورد فعال سازی عصبی ارائه دهد، به ویژه در مراحل اولیه پاسخ BOLD که انعکاس پاسخ سریع از رگ های خونی کوچکتر در مغز به فعالیت عصبی موضعی تصور می شود. به طور سنتی تصور می شد که fMRI برای اندازه گیری نوسانات مغز به دلیل وابستگی سیگنال fMRI به تغییرات آهسته در جریان خون بسیار کند است با این حال، مطالعات اخیر با استفاده از fMRI فوق سریع در 3TوT 7 نوسانات عصبی سریع تا 0.75 هرتز در قشر بینایی را به دنبال تحریک بینایی با فرکانس بالا نشان داده است. اگر چه باید دید که آیا این سیگنالها اطلاعات بیشتری را فراتر از موارد تعبیه شده در نوسانات BOLD آهسته تر حمل میکنند ، امکان به دست آوردن چنین سیگنال هایی نوید کشف غیر طبیعی نوسانات در ساختارهای کوچک عمیق مغز مانند هسته های ساقه مغز را می دهد ،در صورتی که برای تصحیح نویز سریع فیزیولوژیکی باشد، (به عنوان مثال، حرکت قلبی و تنفسی در اطراف ساقه مغز). با توجه به اینکه مشخصه پاتوفیزیولوژیک بیماری پارکینسون تخریب چندین سیستم انتقال دهنده عصبی موجود در ساقه مغز است ، این تکنیک های جدید ممکن است آزمایش برای فعالیت تغییر یافته و اتصال عملکردی این هسته ها در PD و سایر اختلالات عصبی را ممکن کند. نویسنده : حسین ایزی
Conclusions
توسعه فناوری MRI در 20 سال گذشته در کنار زدن محدودیت های قدرت میدان مغناطیسی ساکن و دامنه و سرعت گرادیان متمرکز شده است. پیشرفت در تصویربرداری در میدان فوق العاده بالا، به ویژه درT 7 ، به طور موثر در کیفیت تصویر نسل بعدی برای تصویربرداری عصبی بالینی، با SNR بهتر و اسکن هایی با قدرت تفکیک بالاتر آغاز شده است که تجسم بهتر ضایعات کوچک و ظریف مانند ضایعات قشر مغز در MS و ناهنجاری های قشر مغز در صرع (Epilepsy) را ارائه می کنند. در همان زمان، پیشرفت در تکنولوژی گرادیان ، دریافت تصویر با کیفیت بالا در زمان اسکن کوتاه تر و همچنین وضوح بهتر ریزساختار بافت از طریق MRI انتشار را مقدور کرده است و در مورد هیستوپاتولوژی اجازه می دهد تا برای اولین بار توصیف ویژگی های بافت میکروسکوپی در مغز انسان زنده به موازات چیزی که مستقیماً قابل مشاهده است محقق شود. با تکیه بر موفقیت این پیشرفت ها، در چند دهه آینده احتمالاً شاهد ادامه آن به سمت قدرت میدان حتی بالاتر و سیستم های گرادیان با قدرت بالاتر خواهیم بود ، در حالی که تشویق به گسترش بیشتر پذیرش میدان فوق العاده بالا و تکنولوژی گرادیان فوق العاده بالا و فوق سریع برای استفاده بالینی است.




