دیدگاه های مهم و جدید در زمینه تصویربرداری هسته ای با معرفی سیستم PET/CT در سال ۲۰۰۱ ایجاد شد.حساسیت بالای PET در محدوده picomolar،اجازه تشخیص مقادیر دقیقه ای ازنشانگرهای لیبل شده را در داخل بدن می دهد که در واقع باعث شده PET مدالیته انتخابی برای تصویربرداری مولکولی باشد.
توانایی ترکیب اطلاعات عملکردی PET با رزولوشن بالا و اطلاعات ۳D مورفولوژیک حاصل از CT با یک دستگاه واحد یک مسیر جدید و روشن در تصویربرداری تشخیصی ایجاد کرده است.
در مقایسه با دو مدالیته تصویربرداری مستقل ،ترکیب اسکنرهای PET و CTبر یک گانتری نه تنها باعث انعطاف پذیری و راحتی بیشتر و سرعت بالا در تصویربرداری چند مدالیته می گردد بلکه دقت بالاتری در ثبت داده های حاصل از PET و CT در مقایسه با آنچه به وسیله ی نرم افزار مبتنی بر fusion از مطالعات تصویربرداری که به طور جداگانه به دست آمده است، دارد.
محدودیت های PET/CT و توانایی بالقوه : PET/MR
اگرچه PET/CT به سرعت در حال تبدیل شدن به یک ابزار حیاتی در تشخیص بالینی می باشد اما محدودیت های خاصی نیز دارد:
• در سیستم PET/CT اطلاعات حاصل از PET و CTبه صورت سریالی ((sequential به دست می آید و نه به صورت همزمان.
• در این مورد احتمال ایجاد ارتیفکت به دلیل حرکت بیمار یا ارگان خاص در حین اسکن و یا بین دو اسکن و همچنین به دلیل تفاوت های موجود بین پروتکل های تنفسی مورد استفاده در CT و PET وجود دارد .
این آرتیفکت ها می تواند بر روی دقت ثبت داده ها و تصحیح تضعیف( (attenuation correction تاثیر گذارد و به طور کلی دقت سنجش فعالیت نواحی خاص را به خطر اندازد.
• به علاوه موارد کاربرد بالینی زیادی وجود دارد که تصویربرداری MRنسبت به CT ترجیح داده می شود و از مزایای قابل توجه MRI می توان به کنتراست بالای بافت نرم و عدم استفاده از اشعه یونیزان اشاره کرد.
• ادغام اسکنرهای PET و CT که اجازه دریافت اطلاعات را به طور همزمان دهد مشکل است و نیاز به تکنولوژی خاص آشکارسازهای سازگار با کسب متقارن انرژی پایین ،شار بالای فوتون های X در CT و همچنین استحاله اشعه گاما با انرژی ۵۱۱ Kev برای تصویربرداری PET دارد.
تحقیقات انجام شده در زمینه PET/MR ،امکان اسکن همزمان را در این مدالیته جدید نشان می دهد.دستیابی به داده های PET و MRI به طور همزمان، اساسأ اجازه همبستگی زمانی خوب بین داده های به دست آمده به صورت دینامیک را از دو مدالیته می دهد.
PET/MR می تواند اطلاعات گرفته شده از MR در هردو زمینه آناتومی و عملکردی را برای همبستگی با اطلاعات کمی حاصل از PET در دیگر جنبه های عملکرد بافت ارائه دهد.که این مورد در زمینه تصویربرداری مغز، قلب و عروق و سرطان حائز اهمیت است.
در واقع در تصویربرداری MRI انواع زیادی از پروتکل های انتخابی وجود دارد که باعث افزایش کنتراست و همچنین افتراق بافت های مختلف بدن می گردند و می توانند در تصویربرداری دینامیک با استفاده از ماده کنتراست ،تصویربرداری دیفیوژنی ،fMRI و MR spectroscopy و غیره استفاده گردد.
برای استفاده از این پتانسیل درترکیب PET و MRI برای نمایش چنین اطلاعات چند عملکردی و همچنین آناتومی در بررسی بیماران هرگونه تداخل متقابل بین دو روش تصویربرداری باید از بین برود تا به هر یک از دو روش برای انجام عملکرد مطلوب خود اجازه دهد.
 PET/MR is better for soft tissue that PET/CT and has lower radiation.
PET/MR is better for soft tissue that PET/CT and has lower radiation.
روش های مختلفی برای ترکیب تصویربرداری PETو MR وجود دارد:
Sequential :
ساده ترین روش ، قرار دادن دو اسکنر به صورت سریالی مشابه طراحی اسکنرهای PET/CT می باشد . که در آن هر دو اسکنر PETو MR به ترتیب به صورت دو سیستم مجزا و به عنوان بخشی از یک آزمون استفاده می گردند .
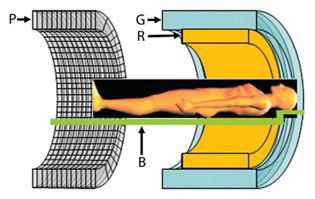
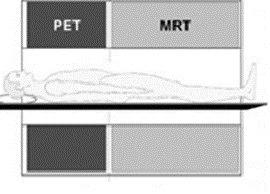
در این نوع طراحی دو مفهوم جداگانه بسته به این که هر دو سیستم تصویربرداری در یک اتاق و یا اینکه در دو اتاق جداگانه قرار گرفته اند وجود دارد.
در طراحی ارائه شده توسط شرکت فیلیپس دو اسکنر PET و MR به صورت متناوبی و به صورت یک دستگاه واحد قرار می گیرد.
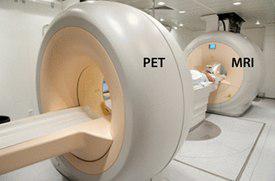
در طراحی که توسط شرکت GE ارائه گردیده در واقع یک نوع تصویربرداری تری مدالیته است که از یک تخت یکسان برای هر دو گانتری در دو اتاق مجزا و انجام ازمون MRI وPET/CT استفاده می شود. این روش نیاز به تغییرات قابل توجهی به خصوص در آشکارسازهای PET دارد برای اینکه به میدان مغناطیسی حساس نباشد و کمترین تأثیر را بر روی عملکرد اسکنر MR بگذارد.
این نوع طراحی از نظر اقتصادی به صرفه است زیرا تغییرات نسبتا کوچکی برای شیلد کردن سیستم PETاز تداخلات میدان مغناطیسی نیاز است و همچنین برای انتقال بیمار از یک واحد تصویربرداری به واحد دیگر به تجهیزات خاصی نیاز نمی باشد.
از محدودیت های این نوع طراحی:
• جمع اوری داده ها به صورت متناوب و نه به صورت موازی و همزمان است که ممکن است سیستم را مستعد ارتیفکت های حرکتی کند.
• به فضایی نسبتا بزرگ برای طراحی سیستم نیاز است
• همچنین برای تصحیح تضعیف داده های حاصل از PET انجام CTنیاز است که باعث افزایش دوز بیمار می گردد.
• به دلیل افزایش زمان جمع اوری داده ها ، ادغام کامل سخت افزار PET درون گانتری MR رویکرد بهتری است .
سه نوع طراحی برای سیستم های تصویربرداری همزمان PET/MR وجود دارد:
• PET insert
• Split field magnet
• Integrated PET/MR imaging
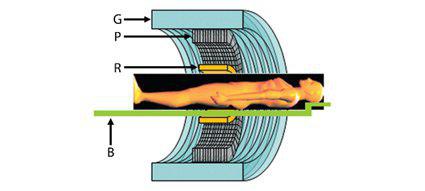 PET insert
PET insert
 split field magnet
split field magnet
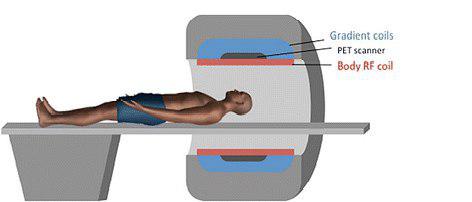 Integrated PET/MR Imaging
Integrated PET/MR Imaging
چالش های مربوط به ترکیب PET وMR :
ترکیب دو تکنولوژی تصویربرداری پیشرفته بدون کاهش عملکرد مطلوب تا حدودی چالش برانگیز است. در هنگام
، چالش های اصلی ادغام سخت افزار به یک دستگاه واحد، مربوط به محدودیت فضای کافی MRI وPET ترکیب
و این واقعیت که آشکارسازهای معمولی PET که از نوع photomultiplier tubes ((PMT هستند در حضور میدان مغناطیسی به درستی عمل نمی کنند.در واقع به علت تداخل میدان مغناطیسی خارجی و ایجاد فشار LORENTZ مسیر الکترون ها بین dynodes در لوله خلا PMT از مسیر طبیعی خود منحرف میشود.

??? Conventional PET detectors are based on scintillation crystal blocks read out by photomultiplier tubes (PMTs)which are highly sensitive to even small magnetic fields )B). These block detectors are standard in current clinical PET scanners. The detector-element map of a position-sensitive PMT-based block detector is completely distorted when a small horse-shoe magnet is placed near the PMT .
موضوع اساسی تداخل متقابل بین دو اسکنر است.که در واقع برای اطمینان از عملکرد پایدار و مطلوب سیستم های PET وMRI ، اینگونه مداخلات باید به حداقل برسد.
اسکنر PETبه دلیل قطعات سخت افزاری مختلف موجود در آشکارساز میتواند باعث ناهمگنی میدان مغناطیسی اصلی( (B0 و میدان مغناطیسی )RF (B1 گردد. از طرفی میدان های گرادیانی MRنیز باعث ایجاد جریان های گردابی (eddy currents ) در مواد رسانا سیستم PET می شود که در نهایت باعث انحراف میدان گرادیانی موثر می گردد. اینگونه مداخلات در نهایت باعث ایجاد آرتیفکت درتصاویر MR و به طور کلی کاهش کیفیت تصویر می گردد.
محدودیت فضا جزء چالش های عمده می باشد:
زیرا اندازه مگنت MRمحدود است بنابراین طراحی سیستم PET برای قرارگیری در داخل مگنت و یا به صورت ادغام کامل با سیستم MR باید به گونه ای باشدکه فضای کافی برای راحتی بیمار موجود باشد.
محدودیت مربوط به فضا همچنین باعث میشود که از منبع انتقال چرخشی (تیوب اشعه X )، منابع نقطه ای پوزیترون و غیره به دلیل طولانی شدن زمان کلی جمع اوری داده ها ،ایجاد اثرات crosstalkبا میدان مغناطیسی و همچنین برای تصحیح تضعیف((attenuation correction استفاده نگردد و تصحیح تضعیف داده های PETباید بر اساس داده های حاصل از MR انجام گیرد که با چالش هایی روبرو است:
در سیستم PET/CT، پدیده تضعیف بر اساس دانسیته الکترونی می باشد و نقشه فاکتور تضعیف برای داده های PET
از طریق تصاویر CT و تبدیل واحد های هانسفیلد به ضرایب تضعیف مربوط به فوتون های با انرژی ۵۱۱Kev که از طریق منحنی های کالیبراسیون خطی به دست می اید، انجام می گیرد.
سیگنال های MR در واقع انعکاسی از دانسیته پروتونی و ویژگی های آسایش بافت می باشد و هیچ ارتباط مستقیمی بین سیگنال اندازه گیری شده در MR و ضرایب تضعیف در انرژی ۵۱۱Kev وجود ندارد.
روش های مبتنی بر MR بر اساس تقسیم بندی بافت های مختلف می باشد که هرکدام به یک ضریب تضعیف خطی از پیش تعیین شده اختصاص داده می شود.
مسئله دیگر اینست که در تصویربرداری MR سیگنال هوا و استخوان شبیه یکدیگر و به صورت حذف سیگنال و تیره دیده می شود.در حالیکه در تصاویر حاصل از PETبیش ترین میزان اختلاف تضعیف را دارند.
نکته بالقوه در تصحیح تضعیف بر اساس MRنسبت به سیستم PET/CT اینست که جمع آوری داده ها می تواند به صورت همزمان باشد اما در PET/CT احتمال mismatch در زمان جمع آوری بین داده های PETو CT وجود دارد.
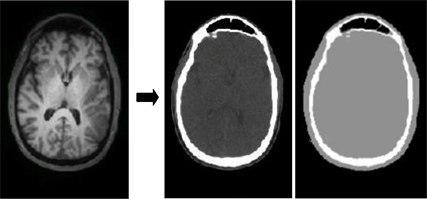
روش های عمده برای تصحیح داده های PET بر اساس MR:
Segmentation Based MRI-AC :
در این روش یک یا چندین تصویر (T1 weighted spin echoes)MR به دست می آید و سپس به نواحی آناتومیک مختلف تقسیم می گردد. توانایی تشخیص نواحی مختلف و طبقه بندی بافتی بستگی به سکانس پالسی مورد استفاده دارد.
مناطق بر اساس شدت سیگنال MR یا محل آناتومیکی خود لیبل گذاری شده( به عنوان مثال شکل ریه ها نیز در نظر گرفته می شود) و ضرایب تضعیف از پیش تعیین شده به آنها اختصاص داده می شود.
تقسیم بندی می تواند به وسیله تکنیک های زیادی از آستانه گیری ساده و عملیات مورفولوژیک گرفته تا روش های پیچیده ترانجام شود.
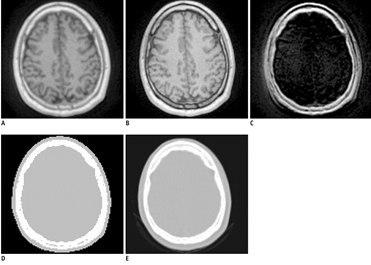
در روش segmentation از سکانس DIXON نیز استفاده می شود که در واقع به افتراق آب و چربی از طریق تصاویر in-phase و out of-phase کمک می کند و اجازه بازسازی تصاویر water-only و fat-only را می دهد و در نهایت یک تقسیم بندی بافتی بر اساس fat-air-soft tissue- lungs ایجاد می شود.
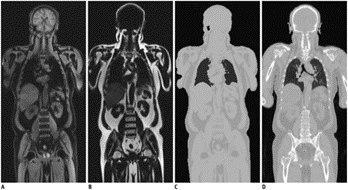 Dixon MRI-based attenuation correction.Dixon water (A) and fat (B) images. C. MRI-based attenuation map generated by combining water and fat images. D. CT of same patient.
Dixon MRI-based attenuation correction.Dixon water (A) and fat (B) images. C. MRI-based attenuation map generated by combining water and fat images. D. CT of same patient.
سکانس DIXON و سایر سکانس های استاندارد قابلیت شناسایی استخوان را ندارند که می توان از سکانس های )Ultra Short Echo Time (UTE استفاده کرد.
در این روش در تصاویر MR، بافت استخوانی با شدت سیگنال بالا دیده می شود.ترکیب تصاویر به دست آمده با TE مختلف اجازه افتراق هوا از استخوان را می دهد.
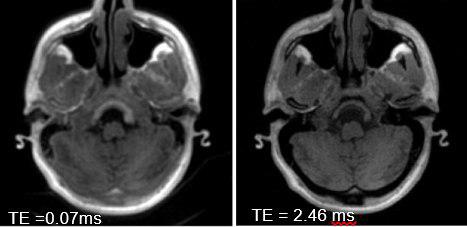
???? Ultrashort echo time (UTE) MRI-based attenuation correction. MR images acquired at first (A) and second (B) echo times (echo time = 0.07 ms and 2.46 ms, respectively). C. Differential image of A and B. D. UTE-based attenuation map. E. CT of same patient.
Template and Atlas based MRI-AC:
این روش بر اساس تعداد مجموعه داده های MRI-CT می باشد که تشکیل یک اطلس را می دهد. تمام تصاویر MR مربوط به اطلس به تصاویر MRدریافتی بیمار، co-register می شود. Atlas-basedیک نقشه تضعیف یا pseudo-CT template در یک قالب آناتومیکی استاندارد به دست می دهد و سپس توسط مدل ها و الگوریتم های خاصی برای fit شدن بر روی تصاویر آناتومیک MR بیمار تنظیم می گردد.
برای به دست اوردن یک قالب استاندارد می توان از تعداد زیادی اسکن هایPET و CTکه در موارد مختلف به دست آمده است و یا همچنین یک میانگیری ساده از اسکن های CT استفاده کرد.
مزیت این روش نسبت به سایر روش ها اینست که می تواند جزئیات ساختاری بیشتری را نمایش دهد و نواحی استخوانی بدون استفاده از UTE شامل می گردد.
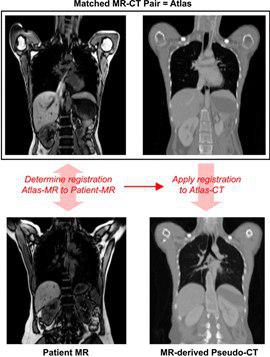
???? Principle of atlas-based MR-AC. The atlas consists of a matching MR-CT image volume that can be generated from a patient. An atlas of attenuation values at 511 keV is generated from matching CT images. The atlas MR image (top left) is coregistered to the MR image volume of a specific patient (bottom left). This transformation is applied to the corresponding CT atlas, thus generating an attenuation image (i.e. pseudo-CT image) that approximately matches the patient anatomy
یک تقسیم بندی از روش های مختلف برای حل مشکل مربوط به حساسیت آشکارسازهای PMTدر میدان مغناطیسی وجود دارد:
OPTICAL FIBERS:
روش استاندارد برای حل مشکل مربوط به PMT و تداخلات بین PET و MR ریا، استفاده از فیبرهای نوری است که به آشکارسازهایscintillation crystals متصل می شوند. بنابراین تنها عناصر تشخیص فوتون های Xو Yدر میدان مغناطیسی اصلی MR قرار می گیرد و PMTs به وسیله فیبرهای نوری به خارج از میدان مغناطیسی انتقال داده می شود.
مطالعات نشان داده است که کریستال های BGO )bismuth germinate) وLSO) lutetium ortho-oxysilicate ) باعث ایجاد اعوجاج کمی در میدان مغناطیسی می شود درحالیکه( (GSO gadolinium orthosilicate وLGSO)lutetium gadolinium orthosilicate)، در مقایسه با بافت بدن استعدادپذیری مغناطیسی مختلفی دارند و باعث اعوجاج و آرتیفکت در تصاویر MR می گردد.
کریستال ها با فیبرهای نوری به ضخامت ۲ mm و طول ۴m به three mu-metal-shielded multi-channel PMTs که در خارج میدان مغناطیسی قرار گرفته اند متصل می گردد.
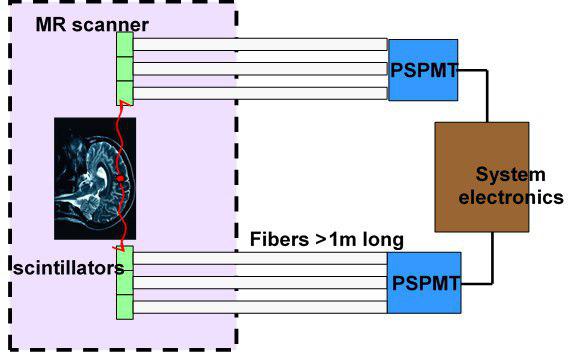
طراحی سیستم PET/MR بر اساس فیبرهای نوری کاستی های خاص خود را نیز دارد:
• هر یک از عناصر کریستال های سوسوزن به یک فیبر نوری متصل می گردد تعداد زیادی گاید نوری نیاز است که با افزایش تعداد آشکارسازها این تعداد نیز زیاد می شود که در نهایت باعث محدودیت سایز Axial FOVدر اسکنر PET بر اساس فیبر نوری می شود.
• از آنجایی که فضای داخل سیستم MR به شدت محدود است استفاده از فیبر نوری باعث کاهش سیگنال نوری در مقایسه با مقدار اصلی موجود در سطح خوانش کریستال می گردد که موجب از دست رفتن زمان و رزولوشن و در واقع کاهش عملکرد کلی سیستم PET می گردد.
Semiconductor light detectors :
یک روش جایگزین PMTs،استفاده از آشکارسازهای سوسوزن حالت جامد مثل avalanche photo diodes( APDs) است.
در APDsمقایسه با PMTsبهره دریافت کمتری دارند و به تغییرات دما حساس تر هستند. با این حال مزیت عمده APDsاین است که:
• نسبت به میدان های مغناطیسی غیرحساس هستند بنابراین می توانند درون میدان مغناطیسی توسط یک گاید نوری کوتاه تر مستقیما به کریستال های سوسوزن متصل شوند .
• از دست رفتن سیگنال نوری به حداقل می رسد و تبدیل نور به سیگنال های الکتریکی در داخل سیستم MR رخ می دهد
• استفاده از فیبر های نوری شکننده و بزرگ را غیر ضروری می سازد.
• APDs نسبت به PMTs کوچکتر هستند بنابراین به یک طراحی با فضای کوچکتر برای سیستم PET/MRمی توان دست یافت که باعث انعطاف پذیری بیشتر در انتخاب سایز Axial FOV و TransAxial درسیستم PET می گردد.
بر این اساس ردیف های متعدد از اشکارسازهای APD می توانند در کنار یکدیگر قرار بگیرند و یک Axial FOVبزرگ را ایجاد کنند( به خصوص برای تصویربرداری کل بدن).
به دلیل توان دریافتی پایین APDs، نیاز به preamplifier با شار حساس برای تقویت سیگنال های آنالوگ با دامنه کم می باشد که در نزدیکی APDs نصب می شود. نکته قابل توجه اینست که قطعات مربوط به سیستم PET درون مگنت به دقت از تداخلات الکتریکی ایجاد شده محافظت گردد. در واقع از محافظ نازک مسی برای جلوگیری از اعوجاج تصویر MRبه دلیل سیگنال های الکتریکی PET استفاده می شود.
هرچند در بعضی تحقیقات القای جریان ناشی از سیستم گرادیانی MR در محافظ مسی مشاهده گردیده که باعث کاهش قدرت موثر گرادیان و تولید گرما داخل مواد محافظ می گردد.
بنابراین ادغام کامل سیستم PETدرون مگنت تا حدودی چالش برانگیز است و نیاز به بررسی دقیق مواد الکترونیکی و مکانیکی دارد.
 The detector-element map of APD-based PET detectors remain undistorted even in the presence of a 7-T magnetic field
The detector-element map of APD-based PET detectors remain undistorted even in the presence of a 7-T magnetic field
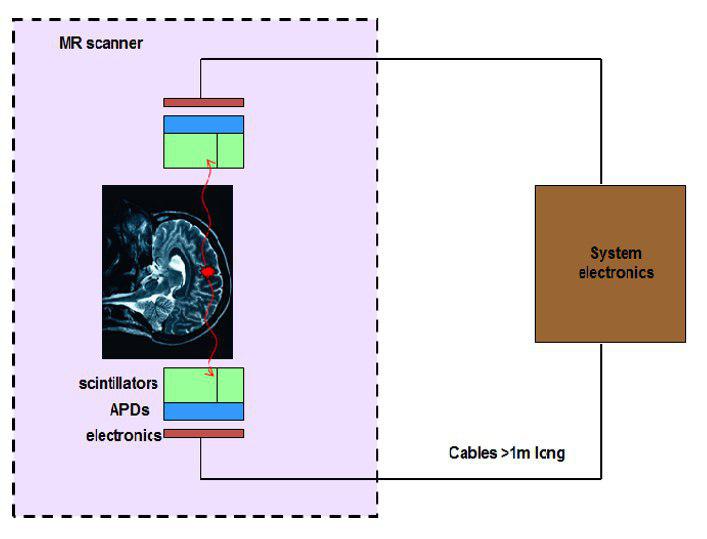
Optical fibers and semiconductor light detectors:
راه کار دیگر ترکیب دو روش فوق با یکدیگر است. به این صورت که از فیبر نوری کوتاه به طول ۱۰ سانتی متر استفاده می شود که سیگنال نوری را از کریستال های LSO به APDs که خارج از میدان دید اسکنر MR قرار گرفته اند هدایت می کند.
در این طراحی هیچ گونه تداخل منفی مشاهده نشده و تصاویر همزمان PET/MR با موفقیت دریافت گردیده است.
از مزایای عمده این گونه طراحی اینست که هیچ گونه مواد فلزی به طور مستقیم درون میدان دید MR قرارنگرفته و استفاده از گاید های نوری کوتاه به اندازه فیبرهای نوری متعدد باعث از دست رفتن سیگنال نمی گردد.
Split Magnet:
رویکرد دیگر برای ترکیب PETو MR به این صورت است که از یک مگنت superconductiveبا یک شکاف حدود ۸۰ میلی متر در وسط مگنت استفاده می گردد که آشکارساز چند حلقه ای با فیبرهای نوری به طول ۱۲۰ سانتی متر در این شکاف قرار می گیرد. گاید های نوری متصل به کریستال های LSOکه در داخل مگنت MR قرار گرفته اند به سمت PMTs حفاظت شده با آهن نرم در بیرون مگنت هدایت می شود.
در این روش فیبرهای نوری در خارج از سیستم MR به جای یک جهت Axialبه صورت شعاعی (Radial) قرار می گیرند.
از محدودیت های این روش کاهش سیگنال نوری و همچنین حفظ همگنی میدان مغناطیسی به شکل مطلوب می باشد.

???? Cutaway schematic of split-magnet of PET/MR imaging shows scintillation crystal ring (vertical arrow), fiber bundles (horizontal long arrow), screened photomultiplier tubes outside magnet cryostat (horizontal short arrow), and split gradient coil (G).
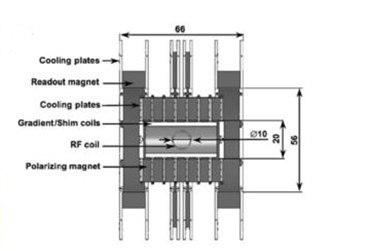
Field Cycling :
مفهوم اساسی این روش جایگزینی میدان مغناطیسی استاتیک با دو میدان کنترل شده دینامیک است. یکی از میدان ها تحت عنوان Polarizing fieldکه معمولا با قدرت میدان ۱T است و برای ساخت مغناطش اصلی استفاده می شود و برای مدت زمان کوتاهی (حدود ۱ثانیه) این میدان اعمال می شود و سپس به سرعت خاموش می گردد.
پس از آن میدان مغناطیسی دوم ( میدان خوانش) روشن می گردد. میدان دوم ضعیف تر است معمولا O.1 T است و زمانی که این میدان روشن است داده ها جمع اوری می گردد.
یکی از مزایای field cycling اینست که که میدان plorizing نیاز به همگنی کامل و خیلی دقیق ندارد و در مقایسه با سیستم های معمول MR به دلیل اختلاف در شدت میدان ها و همچنین زمان اعمال متفاوت باعث کنتراست بهتر تصاویر MR می گردد.
در اینگونه طراحی جمع اوری داده های PET/MRبه صورت sequential می باشد در نتیجه دنبال کردن فرایندهای بیولوژیکی با رزولوشن زمانی بالا با مشکل مواجه می شود.اطلاعات PET زمانی که هر دو میدان خاموش است به دست می آید.
از مزایای اینگونه طراحی اینست که از هیچگونه فیبر نوری استفاده نمی شود و PMTs در مجاورت کریستال قرار گرفته و از کاهش سیگنال جلوگیری می گردد.
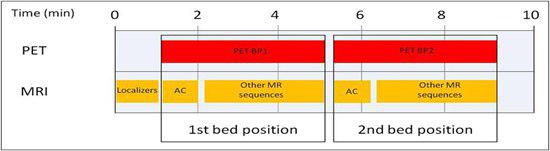
PET/MR protocols:
جمع اوری داده ها در سیستم PET/MR simultaneous معمولا ترکیبی از :
• ۳-۵ حرکت تخت برای تصویربرداری whole body
• به ازای هر حرکت تخت، در ابتدا از سکانس هایVIBE) ) 2-point DIXON 3D volumetric breath hold – و transverse T2 Half-Fourier acquisition single-shot turbo spin echo (HASTE) without contrast agent برای تصحیح تضعیف (MRAC) استفاده می شود.
• زمان جمع آوری داده ها معمولا ۲–۳-minute per bed position
• زمان کل تصویربرداری whole body در حدود ۲۰ min
داده های PET را می توان به صورت همزمان در طول سکانس های اضافی MRدریافت کرد. همچنین بر حسب نوع مطالعه ممکن است به صورت early acquisition، delayed یا dynamic acquisitionباشد.
۱٫ Fast view localizers
۲٫ Dixon AC sequences (all stations)
۳٫ Transverse T2 HASTE (all stations)
۴٫ PET acquisition (simultaneous with #2 and #3) 5. Specific noncontrast or contrast-enhanced sequences based on study indication
کاربردهای بالینی PET/MR:
neurology_ dementia
epilepsy
stoke imaging
oncology_ brain tumors
pelvic tumors
head and neck tumors
Lymphoma
sarcoma
langerhans cell histiocytosis
breast cancers
pediatric imaging
cardiac imaging
musculoskeletal imaging
Oncology:
از آنجایی که کاربرد اصلی PET/CT در زمینه تصویربرداری آنکولوژیک است اکثر مطالعات اولیه به وسیله PET/MR نیز در بررسی مزایای این تکنولوژی جدید دراین زمینه انجام شده است.
کاربرد PET/MR در آنکولوژی برای شناسایی تومورهای سرطانی ،تشخیص متاستازها، بررسی پاسخ به درمان و همچنین تشخیص سریع recurrent tumors قبل از آنکه توسط CT یا سایر مدالیته های تصویربرداری شناسایی شود، می باشد.
در مطالعات انجام شده در زمینه بیماری های مختلف آنکولوژی، امکان انجام simultaneous PET/MR در زمینه بالینی همراه با کیفیت بالای تصاویر و زمان تصویربرداری مطلوب نشان داده شده است .
همچنین در بعضی مطالعات یک سری اطلاعات اضافی که در داده های حاصل از PET/CT به دست نیامده است ،در یافته های حاصل از PET/MR مشاهده شده و در ازریابی نواحی head & neck، liver، urogenital organsو skeleton برتری PET/MR نسبت به PET/CT مشاهده شده است.
در تصویربرداری head & neck ، MRI به دلیل ایجاد کنتراست بالا در بافت نرم ، مدالیته انتخابی می باشد و همچنین یافته ها نشان دهنده ی مزایای FDG-PET با فراهم آوردن اطلاعات متابولیک اضافی و افزایش دقت آزمون MRI در بررسی تومورهای سر و گردن می باشد.
در ارزیابی staging of tumors به وسیله PET/MR به دلیل high spatial and contrast resolution of MRI ،بررسی گسترش تومور و درگیری lymph nodes از بافت سالم اطراف با دقت بالایی انجام می گیرد.
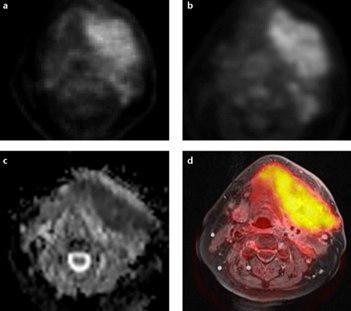
??? Images of a large cancer of unknown primary of the head and neck region derived from PET/MRI. This example demonstrates visually comparable quality of PET/CT (a) and PET/MRI (b) derived PET images. Simultaneous PET/MRI offers the possibility of morphological, functional and metabolic
در زمینه کاربردهای بالینی PET/MR در ناحیه Abdomen به عنوان مثال بررسی تومورهای neuroendocrine حساسیت بالای PET/MR نسبت به PET/CT مشاهده شده.
در ارزیابی متاستازهای کبدی، monitor embolization therapy برای ضایعات کبدی و همچنین ضایعات کبدی کوچکتر از ۱ cm، CT حساسیت و دقت کمتری نسبت به MRI دارد و نقش PET/MR بسیار برجسته است
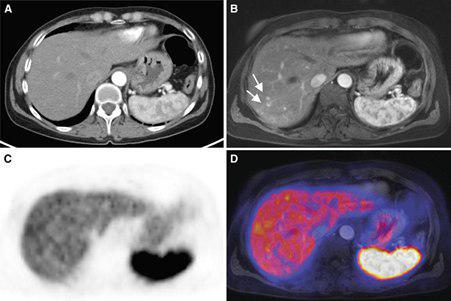
??? ۵۲-year-old female patient with metastatic disease in neuroendocrine tumor. The DOTATATE-PET is shown in C (166 MBq [68Ga]-DOTATATE, 8 min per bed position, 6 min post injection). A Contrast-enhanced CT and B T1 weighted fat suppressed MR image with i.v. contrast in arterial phase. Note the small arterialized lesions in the right liver lobe (arrows) which are neither visualized by CT nor by PET (C). D Superimposition of MRI and PET.
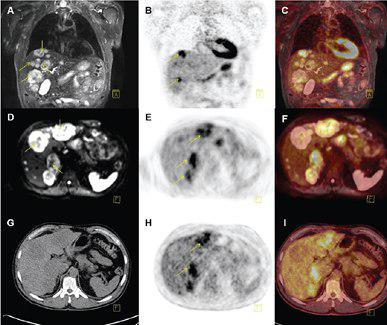
??? A: Coronal T2 weighted STIR MR, B+E: FDG-PET and C: fused PET/ MR illustrating several metastases to the liver, but only some of them PET positive. D-F: Transaxial DWI MRI and FDG-PET illustrating some but not complete overlap between metastases with high signal intensity on DWI MRI and FDG-PET. Finally G-I: illustrates transaxial CT and PET from the PET/CT scanner, with hardly any metastases being visible on the liver on CT-images (not contrast enhanced).
در ارزیابی Pelvic malignancies، به عنوان مثال بررسی prostate cancer به ویژه با استفاده از C-11 choline, F-18 choline or C-11 acetate ، PET/MRنسبت به PET/CT بسیار کارامد بوده است و نکته قابل توجه کاهش دوز بیمار می باشد.
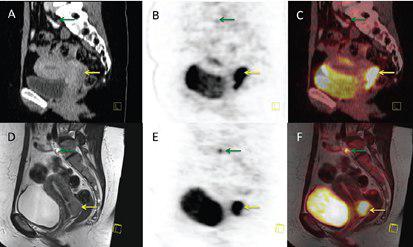
??? A: CT-scan, B: FDG-PET scan performed on the PET/CT scanner, C: Fused PET/CT image –note the mismatch between the bladder on CT and PET due to the difference in uptake time, D: MR-scan, T2 weighted, E: PET scan acquired simultaneous with MR, F: fused PET/MR image –note the perfect fit with bladder on MR and PET.
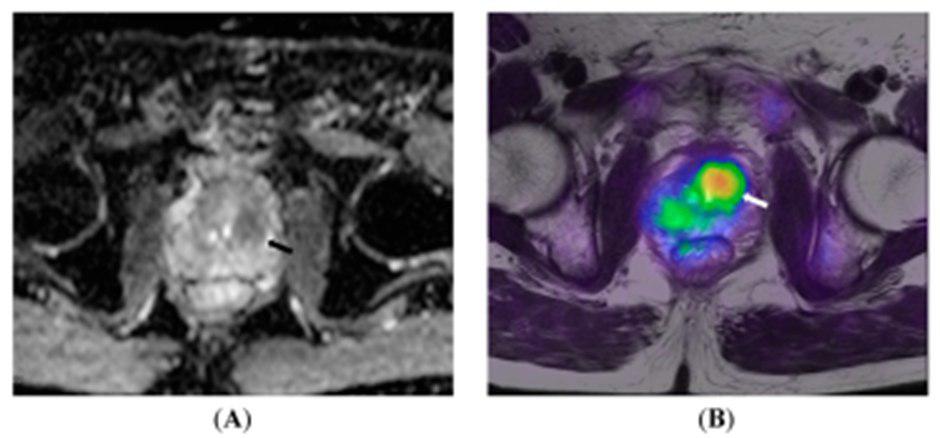
??? A 72-year old patient with prostate cancer. (A) ADC map shows low signal intensity in the central gland (arrow), which is confirmed by 18F-choline PET/MRI (arrow in B) to be metabolically active central gland tumor.
در بررسی متاستازهای استخوانی ، در بعضی مطالعات PET/MR نتایج یکسانی نسبت به PET/CT نشان داده است.
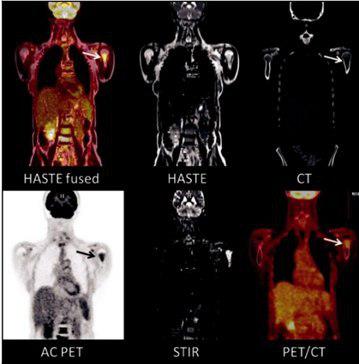 Multiple myeloma. Images depict a focus of metabolically active disease in the left humeral neck that is more conspicuous on MRI than on CT alone (arrows).
Multiple myeloma. Images depict a focus of metabolically active disease in the left humeral neck that is more conspicuous on MRI than on CT alone (arrows).
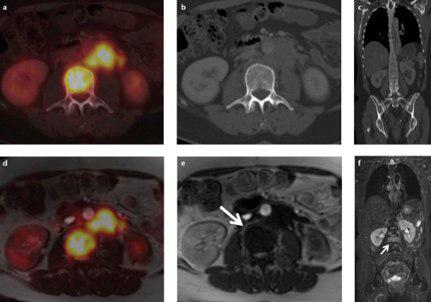
??? A patient with bone metastases originating from ovarian cancer and local bone marrow infiltration in the lumbar spine. While in FDG-PET/CT (a–c) the bone marrow infiltration is only detectable in PET (a) and shows no osseous destruction in CT (b, c), in FDG-PET/MRI (d–f) the infiltration is detectable both in PET (d) and in MRI due to a low signal in T1-weighted sequences (e, arrow) and high signal in T2-weighted sequences (f, arrow). Especially in patients undergoing chemotherapy bone metastases/bone marrow infiltrates might not be FDG-avid and therefore not detectable in PET/CT. In this case PET/MRI might represent an advantage in whole-body imaging.
درارزیابی lung and mediastinal nodal disease، به دلیل دقت تشخیصی بالا در شناسایی و staging اولیه تومورهای ریه و متاستازها و همچنین بیماری های non-small cell cancer، PET/CT مدالیته انتخابی اولیه می باشد.
در بعضی مطالعات اخیر در ارزیابی pulmonary lesions به وسیلهPET/MR ، نتایجی مشابه PET/CT به دست آمده است .در ارزیابی primary lung cancer، انجامPET/MR به دلیل خاصیت multiparametric nature و انجام تکنیک های functional مثل DWI موثر بوده است. با این حال نمی توان PET/MR را جایگزینی برای PET/CT دانست.
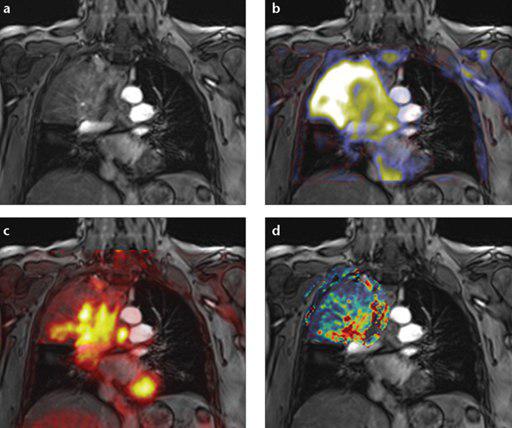
??? Multiparametric simultaneous PET/MRI in a patient with non-small cell lung cancer of the right upper lobe. The contrast-enhanced T1-weighted coronal image (a) is fused with the apparent diffusion coefficient (b), FDG-PET (c) and dynamic contrast-enhanced derived transfer coefficient (d). Multiparametric PET/MRI allows for a more holistic understanding of tumor and tumor stroma, potentially enabling better cancer characterization and therapy control.
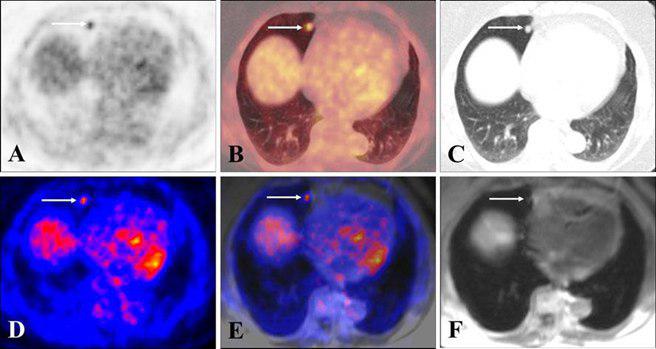
??? Images from a 78-year-old woman with follicular thyroid cancer and lung metastases. Both PETAC_CT (a), PETAC_MR (d) and image fusion with low-dose CT (b) and Dixon T1w (e) show a focal high uptake in the cardiophrenic angle on the right side. c and f illustrate that low-dose CT (c) in the lung window is clearly superior to Dixon T1w (f) in the morphological delineation of the lung nodule which appears very blurry in MR.
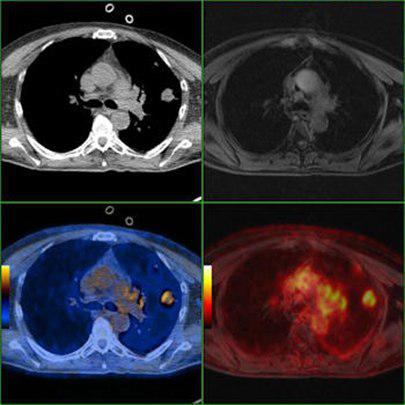 Axial CT and axial PET/CT images show the large metastasis in the left lung.
Axial CT and axial PET/CT images show the large metastasis in the left lung.
The lesion is only detectable in co-registered PET/MRI images but undetectable on the MRI.
Cardiovascular :
در بسیاری از جنبه ها تصویربرداری، noninvasive cardiac MRI به عنوان رفرنس استاندارد در نظر گرفته می شود. در واقع به دلیل کنتراست عالی بافت نرم، spatial resolutionمناسب و همچنین تکنیک های imaging contrast-enhanced، MRI یک ابزار کلینیکی مناسب برای بررسی بافت میوکارد و ناهنجاری های مرتبط با آن می باشد.
به طور کلی کاربرد PET/MR در بررسی بیماری های قلبی-عروقی شامل:
CAD
• Detection of CAD
• Myocardial viability imaging
• Myocardial infarct
• Carotid atherosclerosis
Hereditary, infiltrative and inflammatory cardiovascular diseasessclerosis
• Hypertrophic cardiomyopathy (HCM)
• Amyloidosis
• Cardiac sarcoidosis

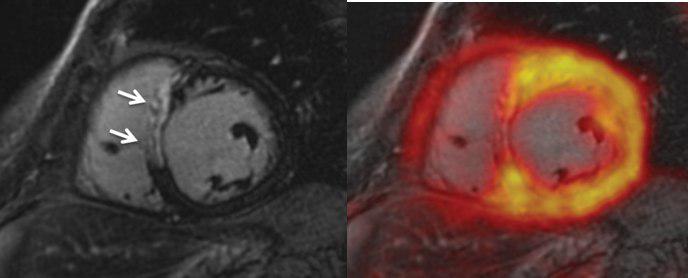
??? A patient with acute myocardial infarction due to occlusion of LAD. Late gadolinium-enhancement reveals transmural septal infarction (a, arrows) that corresponds to a clearly reduced FDG uptake (b).
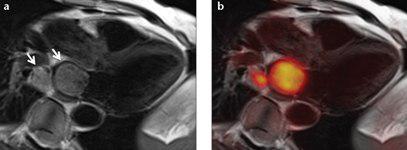
??? A patient with central non-small cell lung cancer infiltrating the left atrium via the lower right pulmonary vein (a, arrows). MR images provide excellent anatomical soft tissue contrast and allow for the detection and quantification of potential impairment of functional parameters like ventricular or valvular function or blood flow. Simultaneous FDG-PET can help in determination of malignancy or differentiation of vital tumor from necrotic tissue or thrombus (b).
Central nervous system:
MRI یک روش منحصر به فرد در تصویربرداری neuro-oncologic است و اجازه مشاهده دقیق تومورها و ضایعات با فراهم آوردن تکنیک هایی مثل dynamic contrast-enhanced imaging، DWI، fMRI، MR spectroscopy را می دهد و کاربردهای گسترده ای در زمینه های زیر دارد:
• Localize epileptogenic focus in patients with epilepsy
• Differentiate Alzheimer’s disease from multi-infarct dementia or depression
• Analyze Parkinson’s disease
• Evaluate extent of stroke and recovery following therapy
با این حال محدودیت هایی مثل تقسیم بندی دقیق glioma و توزیع سلول های glioma در white matter tracts و ارزیابی پاسخ به درمان وجود دارد. PETمی تواند یک رویکرد مولکولی برای مشاهده فرایند های خاص مثل secretion of matrix-metalloproteinases by infiltrating glioma cells یا turnover of radiolabeled aminoacids in vital tumor cells فراهم آورد .
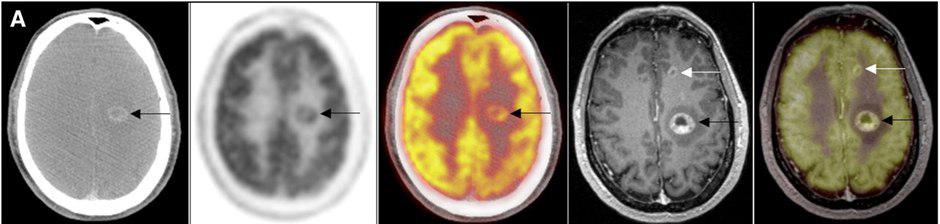
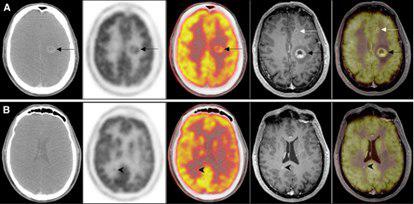
??? Large left-hemisphere metastasis (black arrow) is visible on (from left to right) axial contrast-enhanced CT, 18F-FDG PET, PET/CT, axial contrast-enhanced MRI, and PET/MRI, whereas smaller metastasis of left frontal lobe (white arrow) is visible solely on MRI and PET/MRI. Location of this metastasis directly adjacent to highly 18F-FDG–avid cortex leads to problems with diagnosing this lesion on 18F-FDG PET scan.
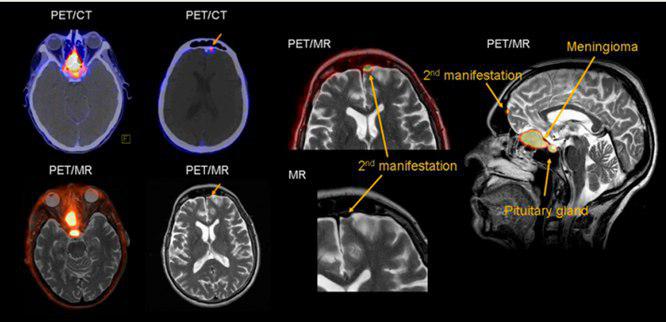
??? PET/CT and PET/MRI 71-y-old woman with frontobasal meningioma in olfactory region. PET/CT images were acquired 20 min and PET/MR
images 100 min after injection of 135 MBq of68 Ga-[1,4,7,10-tetraazacyclododecane-N,N9,N$,N$9-tetraacetic acid]-DPhe1,Tyr3-octreotide. Tracer uptake inthe tumor is seen on PET images. Inaddition, second smaller and previously unknown frontal meningioma was seen on PET and possibly corresponded to small mass demonstrated on T2-weighted turbo spin-echo MR images.This finding was not detected by CT.
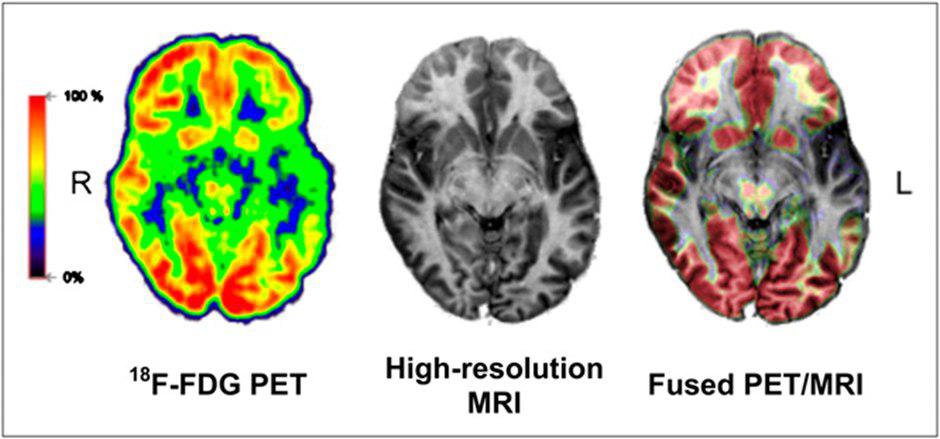
??? Simultaneous PET/MRI study in epilepsy patient. From left to right are shown axial FDG PET, high-resolution MRI scan, and fusion image. Distinct hypometabolism is visible in polar region of left temporal lobe, typically corresponding to epileptogenic focus.
:Pediatric patients and pregnant women
یافته های حاصل از PET/MR با توجه به محدودیت در زمان تصویربرداری طولانی تر نسبت به PET/CT، کاهش قابل توجه دوز بیمار نسبت به PET/CT را نشان داده است.
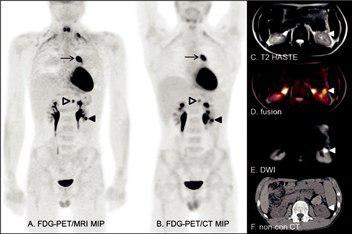
???
B-cell lymphoma undergoing restaging after chemotherapy. Anterior PET/MRI (A) and PET/CT (B) maximal intensity projection (MIP) images show a hypermetabolic focus in the mediastinum (arrow), which was pathologically proven recurrent disease. A hypermetabolic lymph node (open arrow) is also suspicious for disease involvement. A third lesion in the left kidney (solid arrowhead) is difficult to differentiate from collecting system activity on the CT (F); however, axial HASTE (C), fused (D), and diffusion-weighted (E) MR images show that this represents a renal lesion
منبع: گروه تلگرام Optimizing MRI Sequences
تهیه کننده : سرکار خانم برزگر




